|
Es un blog de Jorge Luis Figueroa Apestegui CMP:34170 RNE:031011 UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
viernes, 28 de junio de 2019
lunes, 11 de marzo de 2019
hepatitis autoinmune en la infancia. grupo de trabajo de la sociedad latinoamericana de gastroenterología, hepatología y nutrición pediátrica (slaghnp)
hepatitis autoinmune en la infancia. grupo de trabajo de la sociedad latinoamericana de gastroenterología, hepatología y nutrición pediátrica (slaghnp)
Acta Gastroenterol Latinoam 2016;46: 237-245
Recibido: 13/10/2015 / Aprobado: 24/04/2016 / Publicado en www.actagastro.org el 03/10/2016
Introducción
La hepatitis autoinmune (HAI) es un proceso inflamatorio hepático crónico, de etiología desconocida, que librado a su evolución espontánea puede progresar a cirrosis y enfermedad hepática terminal. Predomina en el sexo femenino y se caracteriza bioquímica y serológicamente por la presencia de transaminasas elevadas, hipergammaglobulinemia y autoanticuerpos circulantes, e histológicamente por hepatitis de interfase. Es fundamental el diagnóstico temprano, ya que el tratamiento inmunosupresor puede salvar la vida del paciente.1-6
Clasificación
De acuerdo con los autoanticuerpos presentes en el suero al momento del diagnóstico, se distinguen 2 tipos de HAI:
- HAI Tipo 1: asociada a autoanticuerpos antinucleares (ANA) y/o antimúsculo liso (smooth-muscle-antibody, SMA), cuya especificidad es mayor si se comprueba que son antiactina y/o antígeno soluble hepático (soluble liver antigen, SLA).
- HAI Tipo 2: asociada a anticuerpos anti-microsomas de hígado y riñón tipo 1 (liver-kidney-microsome-antibody, anti-LKM 1) y/o anti-citosol hepático tipo 1 (liver cytosol, anti-LC1).
El 40% de la HAI tipo 1 y el 80% de la tipo 2 se diagnostican antes de los 18 años de edad (edades promedio 10 y 6,5 años respectivamente). Aunque la mayor prevalencia ocurre en el rango de edad prepuberal, se ha diagnosticado HAI en edades tan tempranas como los 6 meses de vida. Esta enfermedad se observa más frecuentemente en el sexo femenino, con una relación 4:1 para la HAI tipo 1 y 9:1 para la tipo 2.1-5
Patogenia
La HAI es una enfermedad compleja, multifactorial, poligénica, causada por la interacción de factores ambientales con otros causales, en personas con una predisposición genética a desarrollar enfermedades autoinmunes.6
Variantes o polimorfismos genéticos específicos aumentan o disminuyen el riesgo de padecer enfermedades autoinmunes, afectando el fenotipo clínico como ocurre en la HAI tipo 1.7, 8 En la HAI tipo 2, la autorreactividad contra autoantígenos específicos, tales como el citocromo P450IID6 (CYP2D6), es la base patogénica de esta enfermedad.9
El mecanismo que conduce a la destrucción celular y ruptura de la autotolerancia inmunológica es desconocido aunque se sabe que hay una pérdida de la regulación inmune. Se cree que la injuria hepática se produce en respuesta a la presentación de un péptido autoantigénico al receptor de un linfocito T (Th0) mediante las células presentadoras de antígeno (APC) que pueden ser macrófagos, células dendríticas y linfocitos B, en presencia de señales coestimuladoras inducidas por la interacción de los linfocitos CD28 sobre Th0 y los CD80 sobre las APC. El daño hepático está orquestado por los linfocitos CD4 + que reconocen un antígeno propio, que es un péptido ubicado en las APC.10
Para desencadenar la respuesta autoinmune, el péptido se acopla a una molécula de antígeno de histocompatibilidad (HLA) de clase II y es presentado a las células CD4 + Th0 que se activan y se diferencian en Th1 y Th2 en presencia de IL-12 o IL-4, y células TH17 cuando hay un predominio de IL-6. Para desencadenar la respuesta autoinmune, el péptido está acoplado a una molécula de HLA de clase II y presentado a las células Th0, ocurriendo una interacción entre las dos células. Las células Th0 se activan y se diferencian en Th1 y Th2, e inician una cascada de eventos inmunológicos. Los macrófagos presentes en el hígado producen IL-12, las células Th1 secretan principalmente IL-2 e IF-γ, que a su vez activan más macrófagos, aumentan la expresión de moléculas HLA de clase I, incrementándose la vulnerabilidad de los hepatocitos al ataque citotóxico, e inducen la expresión de HLA de clase II sobre los hepatocitos, siendo capaces de presentar el autoantígeno (péptido) a las células Th1, perpetuando de esta forma el ciclo de reconocimiento inmune. Las células Th2, en presencia de un microambiente rico en IL-4, producen IL-4, IL-5 e IL-10, induciendo la producción de autoanticuerpos a partir de linfocitos B y plasmocitos activados. Una vez desencadenada la reacción autoinmune, los hepatocitos son destruidos por diversos mecanismos: directamente en presencia de HLA de clase I, por intermedio de la citotoxicidad de los linfocitos CD8 +, lisis por la acción de citoquinas o por los autoanticuerpos ligados al complemento o por las células NK (asesinas naturales en castellano y natural killer en inglés). Los hepatocitos cubiertos por los autoanticuerpos pueden ser destruidos por la acción del complemento o por el receptor Fc, dos anticuerpos unidos a los linfocitos NK. El proceso de reconocimiento autoantigénico está estrictamente controlado por mecanismos de regulación representados por las células T reguladoras (T-regs) CD4 + y CD25 +.11-14
Una pérdida en las células T-regs conduce a la pérdida de tolerancia inmunológica en HAI y respuestas efectoras inmunes descontroladas.15 Las células T-regs expresan diversos marcadores incluyendo el factor de receptor de TNF inducido por glucocorticoides (GITR, glucocorticoid-induced TNFR family related gene), CTLA- 4 (antígeno 4 del linfocito T citotóxico) y FOXP3. Hay un aumento en la expresión de FOXP3 en la HAI y las células T-regs pueden estar disminuidas en número o reducida su función, generando una interrupción en la modulación de la proliferación de células Th2, con aumento de la producción de citoquinas, lo cual facilita el daño hepático. Además, las células T-regs aumentan la activación de los monocitos, células del sistema inmune innato que abundan en el infiltrado inflamatorio periportal.15-18Los corticosteroides pueden reconstruir la función de las células T-regs y atenuar la respuesta celular citotóxica inmunomediada.
Existe una predisposición genética en la HAI vinculada con los HLA. Variaciones geográficas y los diferentes subtipos de HLA contribuyen a diferentes riesgos relativos de los diferentes grupos étnicos. En Europa y EE.UU., los haplotipos HLA DRB1 / 0301 y DRB1 / 0401 están fuertemente asociados con HAI tipo 1, mientras que la presencia de DR1501 parece ser protectora.19, 20
En Japón domina la fuerte asociación con el haplotipo HLA DR0405, mientras que en América del Sur (Argentina y Brasil) hay un predominio de HLA DR1301 y en menor proporción con DR3 o DR4. La asociación DR7 con HAI tipo 2 se describe en todos los grupos étnicos.21-23
Las deficiencias de IgA y del complemento 4a, condicionadas genéticamente, pueden estar asociadas a HAI.24 La deficiencia de IgA es más frecuente en los pacientes con HAI tipo 2 y está genéticamente vinculada a HLA-DR1 y DR7. Se han observado bajos niveles de complemento 4a en la población pediátrica.25
Otros genes no relacionados con el HLA pueden estar involucrados en la susceptibilidad a la HAI. El antígeno 4 del linfocito T citotóxico (CTLA-4), también conocido como CD152, es una molécula presente en la superficie de los linfocitos T que interactúa compitiendo con los CD28 y los ligandos B7-1 y B7-2 a las APC, transmitiendo una señal inhibidora a las células T. El cambio de adenina (A) por guanina (G) en el exón 1 del gen CTLA- 4 confiere susceptibilidad a algunas enfermedades autoinmunes, incluyendo la HAI en individuos caucásicos en los EE.UU.8 Estos datos no se encontraron en pacientes brasileños con HAI.26 En pacientes de Europa y EE.UU. con HAI tipo 1, se encontró polimorfismo en la posición 308 del promotor del gen del TNFα, en comparación con individuos sanos, asociándoselo con peor respuesta terapéutica. Estos datos no fueron confirmados en pacientes japoneses. Otro polimorfismo en la posición 670 en el promotor del gen FAS se asocia con una progresión de la enfermedad más agresiva.27 Los polimorfismos de los receptores de vitamina D se asocian en la HAI con la activación de los macrófagos, impidiendo la diferenciación de células dendríticas e inhibiendo la función de las células Th1.28
En el 20% de los pacientes con HAI tipo 2 puede asociarse la poliendocrinopatía autoinmune tipo 1 o síndrome APECED (candidiasis crónica mucocutánea, hipoparatiroidismo e insuficiencia adrenal autoinmune). Es una enfermedad autosómica recesiva con múltiples enfermedades autoinmunes órgano-específicas. La enfermedad es causada por mutaciones en el gen AIRE (21q22.3) que codifica para el factor de transcripción AIRE, el cual está implicado en los mecanismos de tolerancia inmune y contribuye a la selección negativa de los linfocitos T autorreactivos en el timo, los ganglios linfáticos y el bazo.29
Diagnóstico
Manifestaciones clínicasLa HAI tipo 2 es más común en niños que en adultos y a pesar de compartir la mayoría de los síntomas clínicos de la HAI tipo I, tiende a ser más severa, manifestándose frecuentemente como un proceso agudo y con mayor tendencia a una rápida progresión a la cirrosis.
Describir un perfil clínico específico es difícil, por la naturaleza fluctuante de la enfermedad. Aproximadamente el 50% de los niños con HAI presentan un cuadro de enfermedad aguda con ictericia, coluria, fiebre, astenia, anorexia y aumento del volumen abdominal. En el 10-15% el comienzo puede ser insidioso, con síntomas inespecíficos como fatiga, náusea, dolor abdominal, artralgias, amenorrea primaria o secundaria. Sin embargo, el espectro clínico es amplio, desde presentaciones asintomáticas a un cuadro agudo severo de insuficiencia hepática aguda.
Al examen físico puede observarse hepatomegalia con o sin esplenomegalia y estigmas de hepatopatía crónica. Ocasionalmente el niño puede presentar ascitis. Los niveles de bilirrubinas séricas usualmente están elevados, así como las aminotransferasas.
La HAI debe sospecharse en todo niño con aparente cuadro de hepatitis aguda, de etiología desconocida, que no presenta mejoría luego de las 4-6 semanas del comienzo de los síntomas. La presentación como insuficiencia hepática aguda suele ser más común en la HAI tipo 2.
Además, los niños pueden presentarse con un proceso crónico descompensado que se asemeja a una insuficiencia hepática aguda (ictericia severa, coagulopatía, encefalopatía), pero asociado a ascitis, circulación colateral y otros elementos clínicos característicos de un proceso crónico, especialmente si el diagnóstico no se ha hecho en una fase temprana.
El efecto de las manifestaciones clínicas tiene impacto en la calidad de vida de los pacientes. Gulati y col realizaron una relación del indicador de calidad de vida vinculado con la salud de un grupo de pacientes con HAI. Este estudio demostró que la fatiga, el dolor abdominal y los aspectos psicológicos intrínsecos eran los elementos que afectaban en mayor medida el diario vivir de estos pacientes.1-6, 30
LaboratorioSi bien no existe ninguna alteración bioquímica específica en la HAI, los hallazgos característicos son:
- Elevación de los niveles de transaminasas entre 2 y 50 veces del valor normal.
- La hipergammaglobulinemia de tipo IgG, que suele ser mayor al 1,5 del valor normal. En la infancia se ha demostrado correlación entre los niveles de IgG y el grado de actividad de la enfermedad. En un 10 a un 20% de los niños puede ser normal.
- La hiperbilirrubinemia y los niveles normales de gamma glutamil transpeptidasa o levemente aumentados, son hallazgos frecuentes.
- El déficit de IgA por debajo de 1,2 gr/l se presenta en el 45% de la HAI tipo 2 y en el 9% de la HAI tipo 1.
- Los niveles de C4 pueden estar disminuidos hasta en el 69% de los casos.
- Leucopenia y pancitopenia se observan en pacientes con cirrosis e hipertensión portal, secundaria a hiperesplenismo.
- La hipoalbuminemia y el déficit de los factores de la coagulación se presentan en los niños con insuficiencia hepática.
- La coagulación puede ser anormal principalmente en la enfermedad crónica avanzada o hepatitis fulminante.1-6, 31-35
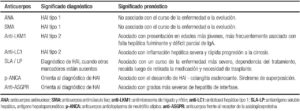
AutoanticuerposEn la HAI los autoanticuerpos ayudan al diagnóstico, pero hay que tener en cuenta que títulos bajos de los mismos e incluso negativos en una determinación, no excluyen el diagnóstico de la enfermedad (Tabla 1).
Los autoanticuerpos circulantes tienen valor diagnóstico y permiten clasificar la HAI en 2 subtipos.
HAI tipo 1
Anticuerpos antinuclearesSe determinan por inmunofluorescencia indirecta (IFI) en secciones de tejidos de riñón, hígado y células gástricas, frente al centrómero, histonas y ribonucleoproteínas. En la mayoría de los casos el patrón es homogéneo y en un porcentaje pequeño puede ser granular o moteado. Está asociado al alelo HLA DRB1 *0401. En el niño se consideran positivos valores igual o mayor a 1/20. Si bien puede encontrarse de manera aislada, suelen asociarse a la presencia de SMA.
Anticuerpos antimúsculo lisoFrente a componentes de actina, tubulina y filamentos intermedios, son detectados en secciones de riñón, estómago e hígado. En riñón tiñe vasos (V), glomérulos (G) y túbulos (T); los patrones VG y VGT son frecuentes en la HAI. A pesar de ser menos prevalentes que los ANA, son más específicos, siendo ésta mucho mayor si se comprueba que son antiactina. En el niño se consideran positivos valores igual o mayores a 1/20.
Se asocian al haplotipo HLA DR3 y tienen cierto carácter pronóstico (peor respuesta al tratamiento). Títulos igual o mayor a 1/320 de SMA casi siempre reflejan la presencia antiactina. El 20% de los pacientes SMA positivos son antiactina negativos, por lo tanto, la ausencia de reactividad antiactina no excluye la HAI tipo 1.
Los anticuerpos ANA y SMA no son específicos de la HAI tipo 1 y pueden encontrarse en otras enfermedades como la hepatitis B y C crónicas, enfermedad de Wilson, niños obesos, etc.1-6, 31-34
HAI tipo 2
Anticuerpos antimicrosomas de hígado y riñón tipo 1Los anti-LKM1 tiñen el citoplasma de los hepatocitos y el túbulo proximal renal.
Son los principales anticuerpos detectados en la HAI tipo 2, altamente específicos y van dirigidos contra el citocromo P450. En niños se considera positivo cualquier valor igual o mayor de 1/10. Se han encontrado presentes en pacientes con hepatitis C crónica, en menos del 5%.
Anticuerpos anticitosol hepático tipo 1Están dirigidos contra la proteína citosólica hepática. Los anti-LC1 pueden acompañar a los anticuerpos anti-LKM1 en la HAI tipo 2, e incluso pueden ser detectados como marcador aislado hasta en un 15% de los pacientes.
Se ha sugerido que su presencia se asocia con la aparición de otras enfermedades autoinmunes, mayor inflamación hepática y una rápida progresión a la cirrosis. No está claro aún si sus títulos se correlacionan con el nivel de actividad de la enfermedad.1-6, 31-34
Anticuerpos antiantígeno soluble hepático/antígeno hepatopancreático (SLA/LP)Frente a citoqueratinas 8 y 18 y glutation S-transferasa y el LP frente a proteínas citosólicas. Presentes hasta en el 60% de los niños con HAI tipo 1. Son del subtipo IgG 1, por lo que se sugiere pueden tener su origen en ciertos estímulos inmunoespecíficos como alguna proteína viral. Parecen mostrar asociación positiva con el alelo HLA DRB1 *0301 y negativa con el HLA DRB1 *04.
Anticuerpos anticitoplasma de neutrófilos atípicos (p- ANCA)Estos anticuerpos presentan un patrón perinuclear atípico, periférico, por IFI y parecen estar dirigidos frente a una proteína de superficie de 50 Kd. Se observan en pacientes con HAI tipo 1. Estos anticuerpos también se detectan en pacientes con colangitis esclerosante primaria y en la enfermedad inflamatoria intestinal, por lo que debe realizarse el diagnóstico diferencial con ellas.
Anticuerpos frente al receptor de la asialoglicoproteína (ASGP-R)Están dirigidos contra una glicoproteína transmembrana de la superficie del hepatocito y probablemente tengan importancia pronóstica. Se encuentran hasta en 1/3 de los niños con HAI y pueden coexistir con ANA, SMA y LKM1. Su presencia se correlaciona con la actividad histológica y su desaparición con la respuesta al tratamiento. Su persistencia se ha asociado con probable recaída tras retirar los corticoides. No son específicos de la enfermedad y pueden estar presentes en hepatitis virales, hepatitis inducidas por drogas y en colangitis esclerosante primaria.
Los anticuerpos ANA, SMA y LKM1 son prácticamente excluyentes entre sí; en los casos excepcionales en que están presentes simultáneamente el niño debe clasificarse como HAI tipo 2.1-6, 31-34
Hallazgos histológicos
Si bien los cambios histológicos de un niño con HAI no son patognomónicos, la biopsia hepática es uno de los pilares en su diagnóstico. Permite caracterizar el compromiso hepático, evaluar el grado de daño del mismo y a la vez descartar otras etiologías. En el diagnóstico histológico es importante el tamaño de la muestra. En general, cuando se trata de una enfermedad difusa se ha planteado que la muestra debe medir 1,5 cm de largo, incluyendo al menos 6 espacios porta. Estudios en adultos con hepatitis crónica han dado cuenta de que muestras pequeñas hacen un sub-diagnóstico del daño hepático, recomendando que la muestra mida 2 cm y contenga 6-8 espacios porta.5, 35, 37-39
El compromiso histológico de la HAI se caracteriza por un infiltrado de linfocitos, células plasmáticas y eosinófilos a nivel del espacio porta, con difusión hacia el lóbulo hepático (zona 2 y 3), infiltración de los hepatocitos de la periferia y erosión de la placa limitante, que es lo que se ha llamado hepatitis de interfase. También se ha descrito como frecuente el hallazgo de emperipolesis, que es la presencia de linfocitos o células plasmáticas intactas dentro de un hepatocito. Por la destrucción y muerte de hepatocitos se observa colapso del tejido conectivo. La regeneración hepática da origen a la formación de rosetas (hepatocitos rodeando un canalículo biliar en el área periportal). La severidad de la hepatitis de interfase es similar en la HAI tipo 1 y 2, sin embargo, la cirrosis es más frecuente en la tipo 1. La presencia de pocas células plasmáticas no descarta la enfermedad.5, 40, 41
Cuando la HAI se presenta como insuficiencia hepática aguda, el hallazgo más característico es el compromiso necroinflamatorio centrolobular. Sin embargo, no hay consenso en los hallazgos histológicos de esta forma clínica grave de la enfermedad.
El diagnóstico diferencial histológico con daño hepático por drogas puede ser difícil; en ambos casos se puede observar hepatitis de interfase, emperipolesis y formación de rosetas, pero son más severos en HAI; al igual que infiltrado de eosinófilos en áreas portales e intra-acinar. Los linfocitos intra-acinar y el daño colestásico son más frecuentes en el daño hepático por drogas. En HAI se encuentra más necrosis focal, confluente y fibrosis que en la causa tóxica. La otra patología autoinmune con la que se plantea diagnóstico diferencial, especialmente en las etapas iniciales, es con la colangitis esclerosante.39, 42, 43
Para objetivar el grado de actividad histológica necroinflamatoria y fibrosis se usa, al igual que en otras hepatitis crónicas, la clasificación de Ishak. Este índice de actividad va de 0-18 evaluando el grado de hepatitis de interfase, necrosis confluente, inflamación focal e inflamación portal, evaluándose además el grado de fibrosis en una escala de 0-6. Este índice también permite objetivar la evolución histológica y la respuesta a tratamiento (Figuras 1, 2 y 3).44-46
Figura 1.

Hematoxilina y Eosina 100X. Espacio porta con hepatitis de interfase linfoplasmocitaria moderada a marcada. Cortesía de los Doctores Marcelo Fabián Amante y Gabriel Casas, Servicio de Anatomía Patológica del Hospital Alemán, Buenos Aires.
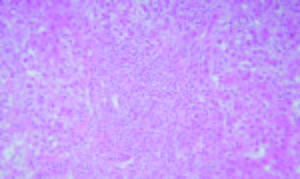
Hematoxilina y Eosina 100X. Espacio porta con hepatitis de interfase linfoplasmocitaria moderada a marcada. Cortesía de los Doctores Marcelo Fabián Amante y Gabriel Casas, Servicio de Anatomía Patológica del Hospital Alemán, Buenos Aires.
Figura 2.

Hematoxilina y Eosina 400X. Sector de interfase con inflamación linfoplasmocitaria y necrosis de hepatocitos con cambios degenerativos asociados y esteatosis focal. Cortesía de los Dres Marcelo Fabián Amante y Gabriel Casas, Servicio de Anatomía Patológica del Hospital Alemán, Buenos Aires.
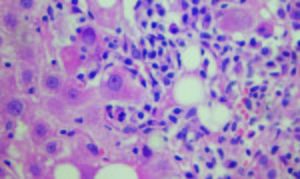
Hematoxilina y Eosina 400X. Sector de interfase con inflamación linfoplasmocitaria y necrosis de hepatocitos con cambios degenerativos asociados y esteatosis focal. Cortesía de los Dres Marcelo Fabián Amante y Gabriel Casas, Servicio de Anatomía Patológica del Hospital Alemán, Buenos Aires.
Figura 3.

Tricrómico 25 X. La tinción de tricrómico destaca la presencia de puentes fibrosos portoportales. Coexiste infiltrado inflamatorio mononuclear en los tractos fibrosos y espacio porta remanentes. Cortesía de los Dres Marcelo Fabián Amante y Gabriel Casas, Servicio de Anatomía Patológica del Hospital Alemán, Buenos Aires.
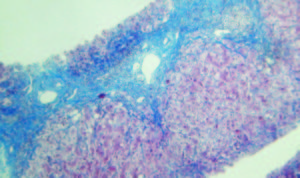
Tricrómico 25 X. La tinción de tricrómico destaca la presencia de puentes fibrosos portoportales. Coexiste infiltrado inflamatorio mononuclear en los tractos fibrosos y espacio porta remanentes. Cortesía de los Dres Marcelo Fabián Amante y Gabriel Casas, Servicio de Anatomía Patológica del Hospital Alemán, Buenos Aires.
Diagnóstico diferencial
En la edad pediátrica debemos descartar además de las hepatitis crónicas virales B o C, la colangitis esclerosante autoinmune, la hepatitis tóxica y la enfermedad de Wilson. La colangitis esclerosante autoinmune comparte el mismo perfil serológico de la HAI tipo 1, pero la primera presenta lesiones de la vía biliar típicas en la colangiografía, lo que permite su identificación.
Hasta el 50% de los pacientes con hepatitis B y C presentan anticuerpos ANA y/o SMA positivos, aunque por lo general en títulos bajos, y hasta un 10% de los pacientes con hepatitis C crónica tienen anticuerpos anti-LKM-1. En estos pacientes, la histología también puede ser similar, pero el grado de inflamación generalmente es menor. La detección de los marcadores virales típicos permite hacer el diagnóstico.
En la enfermedad de Wilson también pueden estar presentes los anticuerpos ANA, y a veces los SMA, en asociación con IgG alta e histología hepática inflamatoria, lo que puede hacer difícil el diagnóstico diferencial con la HAI tipo 1. Los niveles de cobre urinarios, en suero y en el tejido hepático, y la presencia de los anillos de Kayser-Fleischer en el examen oftalmológico con lámpara de hendidura, nos orientan hacia dicho diagnóstico.
En pacientes con presentación aguda, deben además excluirse otras causas virales: hepatitis A y E, citomegalovirus, virus de Epstein-Barr, herpes simple, parvovirus B19 y adenovirus.1-6, 32-35, 46
Tratamiento convencional
El objetivo del tratamiento de la HAI es controlar el proceso inflamatorio del parénquima hepático, con la administración de inmunosupresores. Esta terapia debe iniciarse precozmente, teniendo en cuenta que la rapidez y el grado de respuesta dependen de la severidad de la enfermedad.
El primer esquema terapéutico implementado fue la asociación de prednisona y azatioprina. La prednisona es indicada inicialmente a 2 mg/kg/día (dosis máxima: 40 a 60 mg/d) y la azatioprina a 1,5-2 mg/Kg/día. La dosis de prednisona se reduce gradualmente, siguiendo el descenso de las transaminasas (respuesta terapéutica), con la intención de indicar al paciente la menor dosis capaz de mantener la remisión bioquímica de la enfermedad. La mayoría de los pacientes obtendrán una franca reducción del nivel de transaminasas durante los primeros 2 meses de tratamiento. En algunos casos, la normalización de las mismas será evidente en varios meses más.1-6, 32-36, 46-48
Los efectos adversos relacionados con la administración prolongada de prednisona son: obesidad, hábito cushingoide, estrías cutáneas, hipertricosis, osteopenia/ osteoporosis, diabetes, cataratas, hipertensión arterial, etc. Los vinculados con la administración de azatioprina, aunque infrecuentes, incluyen: colestasis, enfermedad venooclusiva, pancreatitis, toxicidad de médula ósea, etc.
La suspensión del tratamiento inmunosupresor luego de obtenida la remisión y mantenida durante varios años, es un hecho deseable, sin embargo, existen solo reportes anecdóticos. Se menciona una posible discontinuación de la terapia en el 20% de los casos de la HAI tipo 1 pero en ningún niño con la HAI tipo 2.13, 33-37, 46-48
Tratamiento de pacientes no respondedores
Alrededor del 20% de los pacientes con HAI no responden al tratamiento convencional y cerca de un 40% de los respondedores presentan episodios frecuentes de recidivas que requieren un tratamiento alternativo para impedir la progresión de la enfermedad a falla hepática y necesidad de trasplante.
Las alternativas terapéuticas de los casos no respondedores actualmente se basan en drogas inmunosupresoras utilizadas en el post-trasplante para evitar el rechazo celular como el micofenolato mofetil (MMF), inhibidores de la calcineurina y la rapamicina.45
El MMF es un inhibidor de la síntesis de purinas, consiguiendo su efecto inmunosupresor por la disminución en la producción de linfocitos B y T. Se emplea en dosis de 20 mg/kg dos veces al día en aquellos pacientes no respondedores o bien aquellos que no toleran la azatioprina. Los efectos secundarios más comúnmente observados son leucopenia o neutropenia, que a menudo llevan a la necesaria reducción de la dosis o a la suspensión de la medicación. Existen varios reportes de casos sobre el uso del MMF en pacientes refractarios, destacando una serie de 26 pacientes no respondedores al tratamiento clásico, tratados con MMF, seguidos por 5 años, de los cuales el 70% respondió a esta alternativa y manteniéndose con transaminasas normales durante el período de seguimiento.47-49
Si existe intolerancia al MMF o persiste la falta de respuesta, se debe considerar el uso de inhibidores de la calcineurina, tacrolimus o ciclosporina. Éstos deben ser usados con precaución y dosando los niveles en sangre por su potencial toxicidad. Los inhibidores de la calcineurina actúan inhibiendo la expresión del receptor de interleuquina 2 y la expansión de los linfocitos T CD4.
La ciclosporina es un inmunosupresor potente que se ha utilizado efectivamente tanto en niños como en adultos con HAI. En la edad pediátrica se ha demostrado que puede inducir remisión en HAI tipos 1 y 2 al administrarse como tratamiento inicial. Se ha utilizado durante un período de 6 meses, destinado al control del proceso inflamatorio, continuando posteriormente con dosis bajas de prednisona y azatioprina. Se documentó respuesta sostenida en más del 95% de los pacientes con efectos adversos leves y tansitorios.1, 33, 50-53
La rapamicina, un macrólido que inhibe la repuesta a la interleuquina 2 y de esta forma la activación de los linfocitos T y B, también ha sido propuesta para tratamiento de casos de HAI refractaria, aunque la experiencia es limitada.52, 54
Entre las alternativas más recientemente propuestas se encuentra el rituximab. Se trata de un anticuerpo monoclonal quimérico, murino y humano, obtenido por ingeniería genética, que se une específicamente al antígeno CD20, expresado en linfocitos pre-B y B maduros, causando su muerte por apoptosis. El rituximab fue inicialmente aprobado para el tratamiento del linfoma no-Hodgkin y la artritis reumatoidea. Aunque la HAI es considerada una enfermedad autoimmune mediada por células T, las células B han demostrado jugar un rol importante en varias enfermedades autoinmmunes debido a la producción de autoanticuerpos, o como células presentadoras de antígenos, y por la secreción de citoquinas (IL- 2, IF, IL-6). Debido al elevado nivel de IgG y los altos títulos de anticuerpos presentes en HAI, se cree que el rituximab tiene un rol en su tratamiento. Existen algunos trabajos recientemente publicados que demuestran su eficacia en el tratamiento de casos refractarios de HAI con buena tolerancia y un bajo perfil de toxicidad.52, 55-58
El trasplante hepático está indicado en aquellos casos de HAI que se presentan como falla hepática fulminante o bien en los casos en que la enfermedad progresa a insuficiencia hepática terminal a pesar del tratamiento instituido (10-20%), o por abandono del mismo. Luego del trasplante, la tasa de recurrencia de la HAI es cercana al 20%. El diagnóstico de recurrencia se basa en anormalidades bioquímicas, presencia de autoanticuerpos e histología característica. Puede ocurrir varios años post-trasplante; es por ello que se aconseja mantener una dosis de corticoides constante. Debido a la alta tasa de recurrencia y a la intensa inmunosupresión requerida en el post-trasplante en esta situación, es que se deben hacer los mayores esfuerzos para realizar un diagnóstico y tratamiento temprano de la enfermedad con el objeto de evitar, en la mayoría de los casos, la progresión de la misma y la necesidad de trasplante.1-6, 32-37, 59
Agradecimientos. Agradecemos la participación en la revisión bibliográfica de los Doctores Gustavo Boldrini (Argentina), Graciela Caballero (Uruguay), Cristina Galoppo (Argentina) y Violeta Sereno (Uruguay).
martes, 11 de diciembre de 2018
Consenso y Controversia sobre Hepatitis C
En esta actualización se revisan sus aspectos epidemiológicos, preventivos, diagnósticos, evolutivos y terapéuticos.
Autor: Dr. José Luis Fernández * Fuente: Departamento de investigación BioSidus
La hepatitis C es una enfermedad de alta prevalencia. Desde que en 1989 se descubrió el virus de la hepatitis C (HCV) se ha avanzado mucho en el conocimiento de esta enfermedad. Sabemos actualmente que evoluciona en forma silenciosa y crónica hasta constituir un problema de salud creciente en todo el mundo y prioritario en el área de la hepatología. Por este motivo el tema ocupa gran parte de la literatura de la especialidad y cada vez hay más páginas en la red dedicadas a ella.
Se han elaborado varios consensos internacionales y uno nacional que apuntan a unificar los criterios de estudio y tratamiento de la hepatitis C. Sin embargo, quedan puntos oscuros que son importantes a la hora de tomar decisiones: En primer término, el diagnóstico y la prevención no siempre siguen criterios uniformes basados en la evidencia. En segundo lugar, no se conoce completamente la historia natural y la información mediática sobre este aspecto no es equilibrada. Finalmente, el tratamiento dista de ser óptimo, hay varias situaciones especiales en los que no está establecido cuál es el mejor régimen y son insuficientes las evaluaciones de su impacto sobre la calidad de vida, los costos y el beneficio a largo plazo. Por otra parte, aún en las conductas consensuadas, se suelen tomar decisiones siguiendo criterios subjetivos y se realizan tratamientos fuera de los estándares y de las reglas de la investigación clínica.
El objetivo de este trabajo es revisar sumariamente los principales aspectos de la hepatitis C, haciendo hincapié en los consensos establecidos y abordando las controversias desde una perspectiva crítica
La epidemia silenciosa
La prevalencia del HCV oscila entre 0.1 % y 5 % en los diferentes países y se estima que hay 170 millones de portadores crónicos en todo el mundo, hablándose así de una epidemia silenciosa. No hay estudios poblacionales correctamente diseñados que permitan establecer la prevalencia en la Argentina. Se han reportado cifras de 0.7 % a 1.5 % en dadores de sangre pero es sabido que las evaluaciones en esta población subestiman la verdadera prevalencia. En los países industrializados, la hepatitis C da cuenta de 20 % de las hepatitis agudas, 70 % de las hepatitis crónicas, 40 % de las cirrosis terminales, 60 % de los carcinomas hepatocelulares y 30 % de los trasplantes hepáticos.
¿Cómo se trasmite el HCV?
El HCV es un agente que se trasmite por exposición percutánea a la sangre. Hasta no hace mucho tiempo la vía transfusional era la más importante pero había un 30 % de casos en los que no se detectaba la fuente de contagio. Un reciente reporte de los Estados Unidos estableció los siguientes factores de riesgo en 2316 dadores con HCV: drogadicción endovenosa 51 %, transfusiones 17 %, perforaciones en el cuerpo 9 %, sexo con drogadictos endovenosos 6 %, cárcel 3 %, aguja con sangre 2 %, estigmas religiosos 1 %, inmunoglobulina 1 % y ausencia de factor de riesgo 10 %. Si bien el HCV puede trasmitirse tanto sexual como verticalmente, ambas vías de trasmisión tienen un impacto relativamente bajo, a excepción de las personas con sexo promiscuo y las madres que también son portadoras del virus de la inmunodeficiencia humana (HIV). Los pacientes hemodializados y hemofílicos constituyen poblaciones de especial riesgo. En síntesis, la tendencia actual marca una reducción de la trasmisión transfusional a niveles cercanos a cero desde que se controla la sangre con el anticuerpo específico (anti-HCV), una disminución de casos de fuente desconocida desde que se realizan evaluaciones epidemiológicas más precisas y un crecimiento de la drogadicción endovenosa y el sexo promiscuo como factores de riesgo.
¿Cuándo hay que pesquisar el HCV?
Si bien hay consenso internacional, no siempre se cumplen en la Argentina las recomendaciones en cuanto a la pesquisa del HCV. No se recomienda la pesquisa de rutina en la población general y esto incluye la detección prequirúrgica y preocupacional. Tampoco hay evidencias como para recomendarla en las mujeres embarazadas.
Se recomienda pesquisar el HCV solamente en las personas que han recibido sangre o hemoderivados no controlados previamente con anti-HCV, en los pacientes hemofílicos, en los pacientes hemodializados, en los niños de madres con hepatitis C, en los drogadictos endovenosos actuales o pasados y en los dadores de órganos o tejidos.
¿Cómo se previene la trasmisión del HCV?
La prevención se basa en la detección del anti-HCV en la sangre a transfundir, que es ley en la Argentina, y en las medidas universales de bioseguridad para evitar la trasmisión nosocomial. Es importante instruir a los drogadictos endovenosos para que no compartan las jeringas y a las personas que tienen sexo con múltiples parejas para que adopten medidas de barrera. Dada la baja chance de trasmitir el HCV, no se hace ninguna recomendación especial a los pacientes con pareja estable, debiéndoseles informar que tienen sólo 4 % de posibilidad de contagiar a su pareja y dejando a su criterio el uso de medidas precautorias. No hay evidencias para contraindicar el embarazo y la lactancia en las mujeres portadoras del HCV.
El impacto de la infección por HCV
Este es uno de los puntos controvertidos y tiene relevancia para la conducta frente a los pacientes. La controversia proviene de la falta de un completo conocimiento de la historia natural de la enfermedad debido a su lenta progresión, a la carencia de datos prospectivos, a la dificultad para fijar la fecha de comienzo y a la influencia variable de varios cofactores.
¿Es la hepatitis crónica C una enfermedad que progresa inexorablemente a la cirrosis? En ese caso, ¿cuánto tarda en progresar? ¿O algunos pacientes tienen una evolución leve y otros avanzan a formas severas por razones desconocidas?
Historia natural
La figura 1 muestra la evolución de la hepatitis C a partir de 100 pacientes infectados. De ellos, sólo 36 % tienen una evolución progresiva y 10 % a 20 % desarrollan una cirrosis en un tiempo que lleva de 20 a 40 años. Anualmente, el 2 % de los pacientes cirróticos mueren, el 4 % se descompensan, el 2 % requieren un trasplante y el 1% a 4 % desarrollan un carcinoma hepatocelular. Diversos factores pueden contribuir a una evolución desfavorable: El genotipo 1 y la edad al infectarse (mayores de 40 años) tal vez estén entre ellos. Está demostrado que la coinfección con el HIV y el alcohol empeoran el pronóstico.

Vistos desde el punto de vista de la sobrevida, los pacientes infectados por el HCV tienen una sobrevida global del 97 % a los 18 años, similar a la de la población general. La tasa de mortalidad por hepatopatía a los 45 años es de sólo el 5.9 %. Sin embargo, el desarrollo de cirrosis implica una reducción de la sobrevida, siendo de 91 % a los 5 años y de 79 % a los 10 años con cirrosis compensada y de 50 % a los 5 años con cirrosis descompensada.
¿Qué indican estos datos? No cabe duda que la infección por HCV se asocia al desarrollo de cirrosis, enfermedad hepática terminal y carcinoma hepatocelular. De hecho es la primera causa de trasplante hepático en el mundo. Pero también es cierto que el 80 % de los pacientes tienen un curso benigno y a los 20 años se han recuperado, viven con una hepatitis estable y una espectativa de vida similar a la de la población general o mueren de una causa no relacionada con el HCV. El problema es que, hasta la fecha, no se puede predecir qué pacientes evolucionarán en uno u otro sentido.
¿Cómo se trasmite el HCV?
El HCV es un agente que se trasmite por exposición percutánea a la sangre. Hasta no hace mucho tiempo la vía transfusional era la más importante pero había un 30 % de casos en los que no se detectaba la fuente de contagio. Un reciente reporte de los Estados Unidos estableció los siguientes factores de riesgo en 2316 dadores con HCV: drogadicción endovenosa 51 %, transfusiones 17 %, perforaciones en el cuerpo 9 %, sexo con drogadictos endovenosos 6 %, cárcel 3 %, aguja con sangre 2 %, estigmas religiosos 1 %, inmunoglobulina 1 % y ausencia de factor de riesgo 10 %. Si bien el HCV puede trasmitirse tanto sexual como verticalmente, ambas vías de trasmisión tienen un impacto relativamente bajo, a excepción de las personas con sexo promiscuo y las madres que también son portadoras del virus de la inmunodeficiencia humana (HIV). Los pacientes hemodializados y hemofílicos constituyen poblaciones de especial riesgo. En síntesis, la tendencia actual marca una reducción de la trasmisión transfusional a niveles cercanos a cero desde que se controla la sangre con el anticuerpo específico (anti-HCV), una disminución de casos de fuente desconocida desde que se realizan evaluaciones epidemiológicas más precisas y un crecimiento de la drogadicción endovenosa y el sexo promiscuo como factores de riesgo.
¿Cuándo hay que pesquisar el HCV?
Si bien hay consenso internacional, no siempre se cumplen en la Argentina las recomendaciones en cuanto a la pesquisa del HCV. No se recomienda la pesquisa de rutina en la población general y esto incluye la detección prequirúrgica y preocupacional. Tampoco hay evidencias como para recomendarla en las mujeres embarazadas.
Se recomienda pesquisar el HCV solamente en las personas que han recibido sangre o hemoderivados no controlados previamente con anti-HCV, en los pacientes hemofílicos, en los pacientes hemodializados, en los niños de madres con hepatitis C, en los drogadictos endovenosos actuales o pasados y en los dadores de órganos o tejidos.
¿Cómo se previene la trasmisión del HCV?
La prevención se basa en la detección del anti-HCV en la sangre a transfundir, que es ley en la Argentina, y en las medidas universales de bioseguridad para evitar la trasmisión nosocomial. Es importante instruir a los drogadictos endovenosos para que no compartan las jeringas y a las personas que tienen sexo con múltiples parejas para que adopten medidas de barrera. Dada la baja chance de trasmitir el HCV, no se hace ninguna recomendación especial a los pacientes con pareja estable, debiéndoseles informar que tienen sólo 4 % de posibilidad de contagiar a su pareja y dejando a su criterio el uso de medidas precautorias. No hay evidencias para contraindicar el embarazo y la lactancia en las mujeres portadoras del HCV.
El impacto de la infección por HCV
Este es uno de los puntos controvertidos y tiene relevancia para la conducta frente a los pacientes. La controversia proviene de la falta de un completo conocimiento de la historia natural de la enfermedad debido a su lenta progresión, a la carencia de datos prospectivos, a la dificultad para fijar la fecha de comienzo y a la influencia variable de varios cofactores.
¿Es la hepatitis crónica C una enfermedad que progresa inexorablemente a la cirrosis? En ese caso, ¿cuánto tarda en progresar? ¿O algunos pacientes tienen una evolución leve y otros avanzan a formas severas por razones desconocidas?
Historia natural
La figura 1 muestra la evolución de la hepatitis C a partir de 100 pacientes infectados. De ellos, sólo 36 % tienen una evolución progresiva y 10 % a 20 % desarrollan una cirrosis en un tiempo que lleva de 20 a 40 años. Anualmente, el 2 % de los pacientes cirróticos mueren, el 4 % se descompensan, el 2 % requieren un trasplante y el 1% a 4 % desarrollan un carcinoma hepatocelular. Diversos factores pueden contribuir a una evolución desfavorable: El genotipo 1 y la edad al infectarse (mayores de 40 años) tal vez estén entre ellos. Está demostrado que la coinfección con el HIV y el alcohol empeoran el pronóstico.
Figura 1
Sobrevida.Vistos desde el punto de vista de la sobrevida, los pacientes infectados por el HCV tienen una sobrevida global del 97 % a los 18 años, similar a la de la población general. La tasa de mortalidad por hepatopatía a los 45 años es de sólo el 5.9 %. Sin embargo, el desarrollo de cirrosis implica una reducción de la sobrevida, siendo de 91 % a los 5 años y de 79 % a los 10 años con cirrosis compensada y de 50 % a los 5 años con cirrosis descompensada.
¿Qué indican estos datos? No cabe duda que la infección por HCV se asocia al desarrollo de cirrosis, enfermedad hepática terminal y carcinoma hepatocelular. De hecho es la primera causa de trasplante hepático en el mundo. Pero también es cierto que el 80 % de los pacientes tienen un curso benigno y a los 20 años se han recuperado, viven con una hepatitis estable y una espectativa de vida similar a la de la población general o mueren de una causa no relacionada con el HCV. El problema es que, hasta la fecha, no se puede predecir qué pacientes evolucionarán en uno u otro sentido.
Relación médico-paciente
Cuando se descubre una hepatitis C, la alarma de los médicos tratantes, las intervenciones diagnósticas y terapéuticas no siempre necesarias y la información mediática que antepone los aspectos ominosos de la enfermedad suelen convertir a una persona considerada sana hasta ese momento en un paciente que contagiará a cuantos lo rodean e inexorablemente tendrá que recibir un trasplante hepático o morirá de cáncer. De esta manera, una escasa repercusión clínica de la enfermedad va acompañada de un excesivo impacto sobre la esfera psicológica y la calidad de vida.
La información correcta es, por lo tanto, el primer gesto terapéutico ante un paciente con hepatitis C. Debe ser instruido sobre la baja contagiosidad del HCV, las escasas medidas preventivas que deberá tomar y la compatibilidad con una vida de convivencia, laboral, sexual y de planificación familiar normales. El conocimiento actual que se tiene de la hepatitis C permite asegurarle que muy probablemente vivirá tanto como si no fuera portador del HCV y, en el supuesto caso de que su enfermedad progrese y no responda al tratamiento actualmente disponible, la evolución será muy lenta, dando tiempo para aplicar futuros tratamientos.
El segundo gesto es hacer una correcta evaluación del caso, no sólo desde el punto de vista hepatológico sino en el contexto global del enfermo (¿Tiene una edad avanzada o enfermedades intercurrentes que obstaculizan el tratamiento y hacen que un presunto pronóstico desfavorable por el HCV pase a segundo plano?). Para ello deberán usarse los recursos diagnósticos con la mayor economía y la menor agresión posibles (¿Para qué biopsiarlo, por ejemplo, si su edad es avanzada o sus aminotransferasas son normales y no va a ser tratado?).
Finalmente, se evalúa la posibilidad terapéutica y se le plantea al enfermo con todos los potenciales beneficios y riesgos, incluyendo probabilidad de respuesta, efectos adversos, resultado a largo plazo, costos, eventual entrada a una prueba terapéutica controlada y análisis de la información. Hay que tener en cuenta que los pacientes también navegan por la red. La decisión final será, en todos los casos, una decisión común entre el médico y el paciente.
La información correcta es, por lo tanto, el primer gesto terapéutico ante un paciente con hepatitis C. Debe ser instruido sobre la baja contagiosidad del HCV, las escasas medidas preventivas que deberá tomar y la compatibilidad con una vida de convivencia, laboral, sexual y de planificación familiar normales. El conocimiento actual que se tiene de la hepatitis C permite asegurarle que muy probablemente vivirá tanto como si no fuera portador del HCV y, en el supuesto caso de que su enfermedad progrese y no responda al tratamiento actualmente disponible, la evolución será muy lenta, dando tiempo para aplicar futuros tratamientos.
El segundo gesto es hacer una correcta evaluación del caso, no sólo desde el punto de vista hepatológico sino en el contexto global del enfermo (¿Tiene una edad avanzada o enfermedades intercurrentes que obstaculizan el tratamiento y hacen que un presunto pronóstico desfavorable por el HCV pase a segundo plano?). Para ello deberán usarse los recursos diagnósticos con la mayor economía y la menor agresión posibles (¿Para qué biopsiarlo, por ejemplo, si su edad es avanzada o sus aminotransferasas son normales y no va a ser tratado?).
Finalmente, se evalúa la posibilidad terapéutica y se le plantea al enfermo con todos los potenciales beneficios y riesgos, incluyendo probabilidad de respuesta, efectos adversos, resultado a largo plazo, costos, eventual entrada a una prueba terapéutica controlada y análisis de la información. Hay que tener en cuenta que los pacientes también navegan por la red. La decisión final será, en todos los casos, una decisión común entre el médico y el paciente.
Estudio
¿Cómo se estudia un paciente con hepatitis C?
El diagnóstico, estadificación y seguimiento de la hepatitis C se realiza mediante la curva de las aminotransferasas, el anti-HCV, el HCV RNA, la biopsia hepática, la genotipificación, la carga viral, los parámetros de función hepática, los criterios de Child-Pugh, la endoscopía digestiva alta, la ecografía y la alfa fetoproteína. No todos los pacientes con hepatitis C deben ser sometidos a todos los estudios. Es necesario hacer un uso ordenado, racional y costo-efectivo de estos métodos, actitud que, más allá de algunos puntos controvertidos, no se toma sistemáticamente en nuestro medio.
En la mayoría de los pacientes la hepatitis C es diagnosticada en una etapa crónica y compensada de la enfermedad. Menos frecuente es el diagnóstico durante la evaluación de una hepatopatía crónica descompensada y excepcional el diagnóstico durante la hepatitis aguda, que en general es de curso solapado y pasa desapercibida. Cotidianamente, el paciente con hepatitis C llega a la consulta porque se le detectó una elevación de aminotransferasas o un anti-HCV positivo en una pesquisa.
Aminotransferasas, anti-HCV y HCV RNA.: Las aminotransferasas y el anti-HCV por enzimoinmunoensayo son los métodos de evaluación iniciales y en la mayoría de los casos basta con ellos para realizar el diagnóstico. La elevación de las aminotransferasas por encima de una vez y media los valores normales durante más de seis meses, en forma sostenida o en picos, indica cronicidad. La detección del HCV RNA por PCR es un método costoso y no siempre disponible en nuestro medio. Está dirigida a comprobar si una persona con anti-HCV positivo es portadora del virus, especialmente en función del tratamiento y de la evaluación de la respuesta. La figura 2 sugiere un algoritmo para el uso de estos métodos diagnósticos.
Biopsia hepática. Permite establecer el daño hepático, tanto en su grado (inflamación y necrosis) como en su estadío (fibrosis). Ante un paciente con hepatitis crónica C debe plantearse la realización de una biopsia hepática en función del tratamiento. No se recomienda biopsiar a aquellos pacientes que no van a ser tratados.
Genotipificación y carga viral. Tienen utilidad para determinar la duración pero no para decidir el tratamiento y tampoco se necesitan en aquellos pacientes que no van a ser tratados. Hay métodos exactos y estandarizados para determinar cuál es el genotipo de HCV infectante. La determinación de la carga viral, en cambio, carece de estandarización que permita hacer comparables los resultados. Los nuevos métodos comerciales y la expresión de los resultados en unidades internacionales representan un importante avance hacia dicha estandarización.
Otros estudios: Los parámetros de función hepática son imprescindibles para evaluar el estadío clínico de los pacientes y aquellos con cirrosis deben ser estadificados con los criterios de Child-Pugh. La endoscopía digestiva alta sirve para descartar la presencia de várices esofágicas en los casos con sospecha o confirmación histológica de cirrosis. Todos los pacientes cirróticos deben ser seguidos con ecografía y alfa fetoproteína cada seis meses para la detección precoz del carcinoma hepatocelular.

El diagnóstico, estadificación y seguimiento de la hepatitis C se realiza mediante la curva de las aminotransferasas, el anti-HCV, el HCV RNA, la biopsia hepática, la genotipificación, la carga viral, los parámetros de función hepática, los criterios de Child-Pugh, la endoscopía digestiva alta, la ecografía y la alfa fetoproteína. No todos los pacientes con hepatitis C deben ser sometidos a todos los estudios. Es necesario hacer un uso ordenado, racional y costo-efectivo de estos métodos, actitud que, más allá de algunos puntos controvertidos, no se toma sistemáticamente en nuestro medio.
En la mayoría de los pacientes la hepatitis C es diagnosticada en una etapa crónica y compensada de la enfermedad. Menos frecuente es el diagnóstico durante la evaluación de una hepatopatía crónica descompensada y excepcional el diagnóstico durante la hepatitis aguda, que en general es de curso solapado y pasa desapercibida. Cotidianamente, el paciente con hepatitis C llega a la consulta porque se le detectó una elevación de aminotransferasas o un anti-HCV positivo en una pesquisa.
Aminotransferasas, anti-HCV y HCV RNA.: Las aminotransferasas y el anti-HCV por enzimoinmunoensayo son los métodos de evaluación iniciales y en la mayoría de los casos basta con ellos para realizar el diagnóstico. La elevación de las aminotransferasas por encima de una vez y media los valores normales durante más de seis meses, en forma sostenida o en picos, indica cronicidad. La detección del HCV RNA por PCR es un método costoso y no siempre disponible en nuestro medio. Está dirigida a comprobar si una persona con anti-HCV positivo es portadora del virus, especialmente en función del tratamiento y de la evaluación de la respuesta. La figura 2 sugiere un algoritmo para el uso de estos métodos diagnósticos.
Biopsia hepática. Permite establecer el daño hepático, tanto en su grado (inflamación y necrosis) como en su estadío (fibrosis). Ante un paciente con hepatitis crónica C debe plantearse la realización de una biopsia hepática en función del tratamiento. No se recomienda biopsiar a aquellos pacientes que no van a ser tratados.
Genotipificación y carga viral. Tienen utilidad para determinar la duración pero no para decidir el tratamiento y tampoco se necesitan en aquellos pacientes que no van a ser tratados. Hay métodos exactos y estandarizados para determinar cuál es el genotipo de HCV infectante. La determinación de la carga viral, en cambio, carece de estandarización que permita hacer comparables los resultados. Los nuevos métodos comerciales y la expresión de los resultados en unidades internacionales representan un importante avance hacia dicha estandarización.
Otros estudios: Los parámetros de función hepática son imprescindibles para evaluar el estadío clínico de los pacientes y aquellos con cirrosis deben ser estadificados con los criterios de Child-Pugh. La endoscopía digestiva alta sirve para descartar la presencia de várices esofágicas en los casos con sospecha o confirmación histológica de cirrosis. Todos los pacientes cirróticos deben ser seguidos con ecografía y alfa fetoproteína cada seis meses para la detección precoz del carcinoma hepatocelular.
Figura 2
Tratamiento
¿Cómo se trata una hepatitis C?¿A quién tratar y a quién no tratar?
Como se dijo arriba, la identificación del paciente pasible de recibir tratamiento implica evaluar cuidadosamente las indicaciones, contraindicaciones y potenciales beneficios y riesgos. Hay consenso en tratar a los pacientes que tengan entre 18 años y una edad máxima dependiente más del estado general que de la cronología, HCV RNA positivo, elevación crónica de aminotransferasas, biopsia con necroinflamación moderada o severa, con o sin fibrosis, y hepatopatía compensada.
Aunque es un tema de controversia y algunos autores prefieren esperar y ver la evolución en el tiempo, pueden tratarse pacientes con daño histológico leve, especialmente si son jóvenes y tienen una expectativa de vida lo suficientemente larga como para que la enfermedad progrese. Aunque no son concluyentes para el tratamiento que se usa actualmente, hay bastantes evidencias para tratar a los pacientes con hepatitis aguda, con manifestaciones extrahepáticas claramente asociadas al HCV o con una coinfección por HIV en situación estable. En la población pediátrica hay suficiente experiencia con interferón pero no con la combinación utilizada actualmente.
No se tratan pacientes alcoholistas activos, drogadependientes, añosos con comorbilidad severa o cirróticos descompensados. Los casos con aminotransferasas normales no deben tratarse fuera de estudios controlados porque hay estudios mostrando que la progresión espontánea es escasa y la respuesta al tratamiento pobre o contraproducente.
Hay numerosas situaciones clínicas que, cuando son severas, se convierten en contraindicaciones: citopenias, cardiopatías, trastornos psiquiátricos, insuficiencia renal, enfermedades autoinmunes, convulsiones y diabetes. Debido a la probada teratogenicidad de la ribavirina, hay que descartar el embarazo en las mujeres en edad fértil y tanto las mujeres como los hombres deben ejercer una estricta anticoncepción hasta seis meses después de terminado el tratamiento.
¿Cómo se indica el tratamiento?
El esquema estándar para el paciente estándar, consensuado y aprobado por los organismos oficiales, incluído el de la Argentina, es la combinación de interferón alfa (3 millones de unidades tres veces por semana por vía subcutánea) y ribavirina (1000 o 1200 mg diarios por vía oral). Todo otro esquema, incluyendo dosis más altas o diarias de interferón, debe estar sujeto a la investigación en estudios controlados. La ribavirina está contraindicada en los pacientes hemodializados y sólo pueden ser tratados con interferón.
Recientemente se han desarrollado moléculas de interferón unidas a polietilenglicol (interferón pegilado) que aseguran liberación lenta, niveles séricos constantes y administración semanal, con los consecuentes beneficios en la eficacia y la tolerancia.
Próximamente, el tratamiento combinado con interferón pegilado y ribavirina estará aprobado para su uso en la práctica diaria y será el nuevo estándar terapéutico.
Los efectos adversos son numerosos y frecuentes, pueden ser graves y deben ser pesquisados cuidadosamente, en particular el sindrome pseudogripal, la astenia, la anemia por ribavirina, la neutropenia y trombocitopenia por interferón, las infecciones, las alteraciones psiquiátricas y la disfunción tiroidea.
De su gravedad depende que se reduzcan las dosis o se suspenda el tratamiento. La tasa de suspensión por efectos adversos o abandono llega al 20 %.
¿Cuánto tiempo dura el tratamiento?
En este punto hay algunas cuestiones no resueltas. Todo tratamiento dura por lo menos seis meses. A los seis meses se hace una evaluación: Si no se logró una respuesta virológica, se suspende porque no hay posibilidades de una respuesta más tardía. En caso de que haya respuesta, hay que decidir su continuación hasta completar un año y existen dos conductas, sin que esté establecido cuál es la mejor: El Consenso Europeo sugiere tratar seis meses a todos los pacientes con genotipo no 1 y a aquellos con genotipo 1 y carga viral baja, dejando el tratamiento de un año para quienes tienen genotipo 1 y carga viral alta. Un importante trabajo de Poynard y cols. considera los cinco factores favorables de respuesta (edad menor de 40 años, sexo femenino, ausencia de fibrosis o sólo fibrosis portal, carga viral menor de 3.5 millones de copias por ml y genotipo 2 o 3), reservando el tratamiento de seis meses para los pacientes con cuatro o cinco de estos factores y extendiéndolo al año en aquellos con tres o menos.
Esta última postura parece ser la más adecuada a la complejidad de los factores que intervienen en la respuesta pero tiene el inconveniente de que casi la mitad de los pacientes deberán tratarse durante un año (Figura 3).

Figura 3
Como se dijo arriba, la identificación del paciente pasible de recibir tratamiento implica evaluar cuidadosamente las indicaciones, contraindicaciones y potenciales beneficios y riesgos. Hay consenso en tratar a los pacientes que tengan entre 18 años y una edad máxima dependiente más del estado general que de la cronología, HCV RNA positivo, elevación crónica de aminotransferasas, biopsia con necroinflamación moderada o severa, con o sin fibrosis, y hepatopatía compensada.
Aunque es un tema de controversia y algunos autores prefieren esperar y ver la evolución en el tiempo, pueden tratarse pacientes con daño histológico leve, especialmente si son jóvenes y tienen una expectativa de vida lo suficientemente larga como para que la enfermedad progrese. Aunque no son concluyentes para el tratamiento que se usa actualmente, hay bastantes evidencias para tratar a los pacientes con hepatitis aguda, con manifestaciones extrahepáticas claramente asociadas al HCV o con una coinfección por HIV en situación estable. En la población pediátrica hay suficiente experiencia con interferón pero no con la combinación utilizada actualmente.
No se tratan pacientes alcoholistas activos, drogadependientes, añosos con comorbilidad severa o cirróticos descompensados. Los casos con aminotransferasas normales no deben tratarse fuera de estudios controlados porque hay estudios mostrando que la progresión espontánea es escasa y la respuesta al tratamiento pobre o contraproducente.
Hay numerosas situaciones clínicas que, cuando son severas, se convierten en contraindicaciones: citopenias, cardiopatías, trastornos psiquiátricos, insuficiencia renal, enfermedades autoinmunes, convulsiones y diabetes. Debido a la probada teratogenicidad de la ribavirina, hay que descartar el embarazo en las mujeres en edad fértil y tanto las mujeres como los hombres deben ejercer una estricta anticoncepción hasta seis meses después de terminado el tratamiento.
¿Cómo se indica el tratamiento?
El esquema estándar para el paciente estándar, consensuado y aprobado por los organismos oficiales, incluído el de la Argentina, es la combinación de interferón alfa (3 millones de unidades tres veces por semana por vía subcutánea) y ribavirina (1000 o 1200 mg diarios por vía oral). Todo otro esquema, incluyendo dosis más altas o diarias de interferón, debe estar sujeto a la investigación en estudios controlados. La ribavirina está contraindicada en los pacientes hemodializados y sólo pueden ser tratados con interferón.
Recientemente se han desarrollado moléculas de interferón unidas a polietilenglicol (interferón pegilado) que aseguran liberación lenta, niveles séricos constantes y administración semanal, con los consecuentes beneficios en la eficacia y la tolerancia.
Próximamente, el tratamiento combinado con interferón pegilado y ribavirina estará aprobado para su uso en la práctica diaria y será el nuevo estándar terapéutico.
Los efectos adversos son numerosos y frecuentes, pueden ser graves y deben ser pesquisados cuidadosamente, en particular el sindrome pseudogripal, la astenia, la anemia por ribavirina, la neutropenia y trombocitopenia por interferón, las infecciones, las alteraciones psiquiátricas y la disfunción tiroidea.
De su gravedad depende que se reduzcan las dosis o se suspenda el tratamiento. La tasa de suspensión por efectos adversos o abandono llega al 20 %.
¿Cuánto tiempo dura el tratamiento?
En este punto hay algunas cuestiones no resueltas. Todo tratamiento dura por lo menos seis meses. A los seis meses se hace una evaluación: Si no se logró una respuesta virológica, se suspende porque no hay posibilidades de una respuesta más tardía. En caso de que haya respuesta, hay que decidir su continuación hasta completar un año y existen dos conductas, sin que esté establecido cuál es la mejor: El Consenso Europeo sugiere tratar seis meses a todos los pacientes con genotipo no 1 y a aquellos con genotipo 1 y carga viral baja, dejando el tratamiento de un año para quienes tienen genotipo 1 y carga viral alta. Un importante trabajo de Poynard y cols. considera los cinco factores favorables de respuesta (edad menor de 40 años, sexo femenino, ausencia de fibrosis o sólo fibrosis portal, carga viral menor de 3.5 millones de copias por ml y genotipo 2 o 3), reservando el tratamiento de seis meses para los pacientes con cuatro o cinco de estos factores y extendiéndolo al año en aquellos con tres o menos.
Esta última postura parece ser la más adecuada a la complejidad de los factores que intervienen en la respuesta pero tiene el inconveniente de que casi la mitad de los pacientes deberán tratarse durante un año (Figura 3).
Figura 3
Evaluación de la respuesta.
Hay consenso en que la evaluación de la respuesta se basa en la negativización del HCV RNA (respuesta virológica), siendo esta válida cuando se mantiene seis meses después de concluído el tratamiento (respuesta virológica sostenida). Los pacientes con respuesta virológica sostenida tienen una posibilidad de recaer a largo plazo inferior al 5 % y, dado que en esta situación la enfermedad se estabiliza en su evolución, puede hablarse de una situación cercana a la curación. La respuesta bioquímica (normalización de las aminotransferasas) generalmente se asocia a la virológica y tiene un valor relativo en los escasos casos en los que se da aislada. Fuera de protocolos establecidos, no se recomienda la evaluación histológica luego del tratamiento.
Con la combinación de interferón y ribavirina tienen una respuesta virológica sostenida el 35 % a 40 % de los pacientes que inician un tratamiento, tanto los que nunca fueron tratados como los que recayeron a una monoterapia previa con interferón. De acuerdo con un reciente estudio controlado en pacientes vírgenes de tratamiento, esta respuesta puede ascender al 54 % usando la combinación de ribavirina e interferón pegilado.
La posibilidad de respuesta virológica sostenida con esta combinación es de alrededor del 16 % en los pacientes que no tuvieron ninguna respuesta a una monoterapia previa con interferón y de alrededor del 17 % en los que tienen una biopsia con cirrosis. Si bien son cifras bajas, se considera como la única opción terapéutica razonable para estos casos hasta tanto se comprueben los mejores resultados obtenidos en algunos estudios controlados con otros esquemas o con interferón pegilado.
Tratamientos venideros.
Los próximos meses estarán signados por el advenimiento del interferón pegilado y su combinación con ribavirina. Otras drogas, como amantadina, timosina o interleuquina 10, aún no han demostrado claramente su eficacia y se desaconseja su uso fuera de la investigación. A nivel básico se están desarrollando drogas dirigidas a bloquear algún mecanismo de la replicación del HCV, como los inhibidores de proteasa y helicasa, pero no se avizora aún su uso clínico.
Efectos del tratamiento a largo plazo.
La experiencia a largo plazo se basa en la monoterapia con interferón y no es completamente extrapolable a las nuevas opciones terapéuticas. Se sabe que la respuesta al tratamiento trae aparejada la probable erradicación definitiva del virus, una mejor calidad de vida, una mejor función hepática y una mejoría histológica cuyo alcance a la fibrosis es discutido. El tratamiento parece mejorar el curso clínico en algunos pacientes cirróticos y resulta costo-efectivo para las formas leves. Sin embargo, no hay un efecto probado sobre la sobrevida y sobre el riesgo de desarrollar un carcinoma hepatocelular.
Con la combinación de interferón y ribavirina tienen una respuesta virológica sostenida el 35 % a 40 % de los pacientes que inician un tratamiento, tanto los que nunca fueron tratados como los que recayeron a una monoterapia previa con interferón. De acuerdo con un reciente estudio controlado en pacientes vírgenes de tratamiento, esta respuesta puede ascender al 54 % usando la combinación de ribavirina e interferón pegilado.
La posibilidad de respuesta virológica sostenida con esta combinación es de alrededor del 16 % en los pacientes que no tuvieron ninguna respuesta a una monoterapia previa con interferón y de alrededor del 17 % en los que tienen una biopsia con cirrosis. Si bien son cifras bajas, se considera como la única opción terapéutica razonable para estos casos hasta tanto se comprueben los mejores resultados obtenidos en algunos estudios controlados con otros esquemas o con interferón pegilado.
Tratamientos venideros.
Los próximos meses estarán signados por el advenimiento del interferón pegilado y su combinación con ribavirina. Otras drogas, como amantadina, timosina o interleuquina 10, aún no han demostrado claramente su eficacia y se desaconseja su uso fuera de la investigación. A nivel básico se están desarrollando drogas dirigidas a bloquear algún mecanismo de la replicación del HCV, como los inhibidores de proteasa y helicasa, pero no se avizora aún su uso clínico.
Efectos del tratamiento a largo plazo.
La experiencia a largo plazo se basa en la monoterapia con interferón y no es completamente extrapolable a las nuevas opciones terapéuticas. Se sabe que la respuesta al tratamiento trae aparejada la probable erradicación definitiva del virus, una mejor calidad de vida, una mejor función hepática y una mejoría histológica cuyo alcance a la fibrosis es discutido. El tratamiento parece mejorar el curso clínico en algunos pacientes cirróticos y resulta costo-efectivo para las formas leves. Sin embargo, no hay un efecto probado sobre la sobrevida y sobre el riesgo de desarrollar un carcinoma hepatocelular.
Conclusiones
Afortunadamente, el consenso es mayor que la controversia y permite iniciar con optimismo este siglo en el que la hepatitis C será un problema creciente para la salud mundial. La prevención transfusional ha sido muy eficaz y otro tanto se espera de las medidas universales de bioseguridad y de las precauciones en los grupos de riesgo.
El alto costo y la inconstante disponibilidad de los procedimientos necesarios para el diagnóstico y seguimiento de la enfermedad hacen necesario su uso racional. Con los recursos disponibles en la actualidad puede hacerse una adecuada aproximación a las personas infectados por el HCV y, si bien no se conoce completamente la historia natural, lo conocido es tranquilizador para enfrentar cada caso individual, sin que esto, paradójicamente, le reste importancia a las serias consecuencias que puede tener la hepatitis crónica. La información, evaluación y decisión del tratamiento correctas y personalizadas son esenciales para el manejo de estos pacientes.
Cabe preguntarse para qué se hace lo que se hace en materia terapéutica y confrontar la pregunta con las dudas sobre la evolución a largo plazo. ¿Modifica realmente el tratamiento la historia natural de la hepatitis C? Después de una década de desalentadora experiencia con el interferón como monoterapia, los tratamientos combinados estándar con interferón y ribavirina y venidero con interferón pegilado y ribavirina están asegurando mejores posibilidades de respuesta y, consecuentemente, mayores probabilidades de cambiar el curso espontáneo de la enfermedad.
Los desafíos futuros son predecir qué pacientes evolucionarán desfavorablemente; establecer cuáles son los factores predictivos de respuesta y los mejores esquemas para optimizar el tratamiento; desarrollar nuevas drogas más específicas, eficaces, seguras y baratas; y, finalmente, descubrir una vacuna que permita erradicar la infección por el HCV.
* Hepatólogo. Área de Investigación Clínica, Bio Sidus, Buenos Aires.
El alto costo y la inconstante disponibilidad de los procedimientos necesarios para el diagnóstico y seguimiento de la enfermedad hacen necesario su uso racional. Con los recursos disponibles en la actualidad puede hacerse una adecuada aproximación a las personas infectados por el HCV y, si bien no se conoce completamente la historia natural, lo conocido es tranquilizador para enfrentar cada caso individual, sin que esto, paradójicamente, le reste importancia a las serias consecuencias que puede tener la hepatitis crónica. La información, evaluación y decisión del tratamiento correctas y personalizadas son esenciales para el manejo de estos pacientes.
Cabe preguntarse para qué se hace lo que se hace en materia terapéutica y confrontar la pregunta con las dudas sobre la evolución a largo plazo. ¿Modifica realmente el tratamiento la historia natural de la hepatitis C? Después de una década de desalentadora experiencia con el interferón como monoterapia, los tratamientos combinados estándar con interferón y ribavirina y venidero con interferón pegilado y ribavirina están asegurando mejores posibilidades de respuesta y, consecuentemente, mayores probabilidades de cambiar el curso espontáneo de la enfermedad.
Los desafíos futuros son predecir qué pacientes evolucionarán desfavorablemente; establecer cuáles son los factores predictivos de respuesta y los mejores esquemas para optimizar el tratamiento; desarrollar nuevas drogas más específicas, eficaces, seguras y baratas; y, finalmente, descubrir una vacuna que permita erradicar la infección por el HCV.
* Hepatólogo. Área de Investigación Clínica, Bio Sidus, Buenos Aires.
miércoles, 21 de noviembre de 2018
Tumores hepáticos sólidos comunes
Tumores hepáticos sólidos comunes
Esta revisión analiza las diversas características de las lesiones hepáticas sólidas más comunes y las recomendaciones prácticas para el diagnóstico Autor: Dres. Nimer Assy, Gattas Nasser, Agness Djibre, Zaza Beniashvili, et al World J Gastroenterol 2009 July 14; 15(26): 3217-3227
Introducción
Cada vez se identifican más los tumores hepáticos debido al uso generalizado de las técnicas de imagen como la ecografía, la tomografía computarizada (TC) y la resonancia magnética (RM). La mayoría de estas lesiones son detectadas incidentalmente en pacientes asintomáticos. Una historia detallada y la exploración física son esenciales para el diagnóstico y el tratamiento de los tumores sólidos del hígado. Por ejemplo, el uso de anticonceptivos orales o de esteroides anabólicos podría estar relacionado con el adenoma hepático; el consumo de alcohol y la exposición ocupacional se asocian con el angiosarcoma mientras que la colangitis esclerosante primaria, la fasciola hepática, la enfermedad de Caroli y los quistes del colédoco lo hacen con el colangiocarcinoma.
El examen físico debe buscar la sensibilidad del hígado y los signos de hepatopatía crónica o de deterioro general (fiebre, pérdida de peso). La fosfatasa alcalina y la deshidrogenasa láctica elevadas, la albúmina baja, el tiempo de protrombina elevado y la sobrecarga de hierro no son específicos, pero podrían hacer sospechar hepatitis crónica, cirrosis o un proceso infiltrante. El antecedente de hepatitis B o C o de cirrosis puede orientar hacia el hepatocarcinoma (HC). Una neoplasia previa o un tratamiento quimioterapéutico aumentan la sospecha de metástasis hepáticas.
Estado actual de los conocimientos
En la mayoría de los pacientes se puede realizar el diagnóstico adecuado por las características de las imágenes (en general, las lesiones <1,0 cm. son benignas). A los fines diagnósticos, los nódulos hepáticos se diferencian entre los que ocurren en pacientes con cirrosis y pacientes sin cirrosis. Hasta que se demuestre lo contrario, un tumor hepático en un hígado cirrótico debe ser considerado un HC; los tumores hepáticos múltiples en un hígado cirrótico indican HC difus o, en raras ocasiones, los nódulos con un grado elevado de displasia, un linfoma hepático.
En más del 20% de la población en general se hallan lesiones hepáticas benignas, incluyendo el angioma (4%), la hiperplasia nodular focal (0,4%) y adenomas hepáticos (0,004%). Las lesiones hepáticas múltiples en un hígado normal por lo general indican un hígado metastático (el más común, del adenocarcinoma, colon, estómago, pulmón o próstata), pero podrían ser quistes o hemangiomas. Es raro hallar metástasis hepáticas en un hígado cirrótico. Las lesiones hepáticas múltiples de naturaleza benigna como los hemangiomas o la hiperplasia nodular focal, no son infrecuentes en un hígado normal.
Diagnóstico clínico diferencial de la mayoría de los tumores hepáticos
Diagnóstico clínico diferencial de la mayoría de los tumores hepáticos
| . | Hígado cirrótico | Lesiones comunes | Hígado no cirrótico | Lesiones comunes |
| Tumores malignos | Carcinoma hepatocelular Colangiocarcinoma Nódulo hiperplásico de alto grado Linfoma Metástasis (excepcional) | a.d | Metástasis HC bien diferenciado HC fibrolamelar Colangiocarcinoma Hemangioendotelioma Linfoma Melanoma Tumor neuroendocrino Sarcoma(angiosarco-ma, leiomiosarcoma) | a.b a.b.c.g g a g |
| Tumores benignos | Displasia de bajo grado Hígado graso focal Hemangioma Adenoma hepático | d g | Hemangioma Hiperplasia nodular focal Adenoma hepático Hiperplasia regenerativa nodular Transformación nodular parcial Infiltración grasa focal Adenoma del conducto biliar | b a.b a,b b,f e,f c,.e |
a: tumor hepático hipervasularizado. b: tumores extremadamente raros en la cirrosis pero relativamente frecuentes en el hígado normal. c: tumores frecuentes en el lóbulo izquierdo, d: principalmente en cirrosis; e: se hallan por igual en hígado cirrótico y no cirrótico. f: clínicamente semeja la cirrosis. g: tumores extremadamente raros.
Las calcificaciones no tienen ninguna utilidad diagnóstica, pero podrían indicar un carcinoma fibrolamelar o un adenocarcinoma colorrectal, mientras que la hemorragia dentro de la lesión sugiere un adenoma. El primer paso en la cirrosis es la determinación de la α-fetoproteína (AFP) seguida de una ecografía, TC con contraste o RM. Podría ser necesaria la biopsia del núcleo con aguja fina pero se recomienda evitar la biopsia en las lesiones potencialmente operables.
Valor diagnóstico de los marcadores tumorales
La alfa-fetoproteína (AFP), la PIVKA 2 (Protein Induced by Vitamin K Absence: < 0,1 U/ mL.), la desgammacarboxi protrombina y el CA 19-9 (<37 U/mL) son marcadores tumorales para el HC. La AFP es la primera elección para el diagnóstico del HC, siendo el cut-off de 10 ng./ml. La fórmula (Ca 19-9 + CEA × 40) proporciona un índice de exactitud del 86% para el diagnóstico de colangiocarcinoma. Los valores de AFP >400 ng./mL. son indicativos de HC. El 30% de los pacientes con HC <2 cm. tiene AFP normal, el 20% de los pacientes con HC no produce AFP mientras que presencia de nódulos de regeneración o de cirrosis viral son frecuentes los niveles de 20-250.
Un aumento de la AFP es prácticamente diagnóstico de HC. A nivel mundial, el 88% de los pacientes con cáncer comprobado presentó una elevación de la concentración sérica de al menos uno de los marcadores tumorales. La elevación fue notable en el 57%. En cambio, no se hallaron alteraciones de los marcadores tumorales en ninguno de los pacientes con lesiones benignas. Las lesiones iniciales pueden tener marcadores elevados en menos del 30% de los casos.
Técnicas por imágenes
La utilización de una sola modalidad de imagen solo puede ser suficiente para controlar la progresión de la enfermedad, como las metástasis. Los hemangiomas son a menudo diagnosticados por una única modalidad con contraste dinámico para mejorar la imagen. Cuando se requieren otras imágenes para planificar una operación se cuenta con la TC, la angiografía por TC, la RM y la TC contrastada. Si no se dispone de estas técnicas, entre el paciente y el médico deben decidir si se hará una biopsia o una derivación a un centro de estudios por imágenes para realizar estudios por imágenes adicionales.
Las técnicas por imágenes para la evaluación del tumor hepático incluyen:
1) Evaluación del tumor
• Angiografía
• Gammagrafía con eritrocitos marcados
• TC con contraste
• Porto-angiografía con TC (muy sensible para las lesiones secundarias pero solo aplicables a casos seleccionados)
• Ecografía Doppler color
• Ecografía con contraste
• Gammagrafía con eritrocitos marcados
• TC con contraste
• Porto-angiografía con TC (muy sensible para las lesiones secundarias pero solo aplicables a casos seleccionados)
• Ecografía Doppler color
• Ecografía con contraste
2) Evaluaciön de la función del hepatocito y la excreción biliar
• RM con Mn-DPDP (manganeso (II) N,N ‘-dipyridoxylethylenediamine-N,N’-diacetate 5,5 ‘-bis(phosphate) (DPDP)
• RM con gadolinio BOPTA- EOB DTPARM contrastada con dimeglumina
• EOB DTPA
• RM con gadolinio BOPTA- EOB DTPARM contrastada con dimeglumina
• EOB DTPA
3) Evaluación de caLcificaciones tumorales
• Radiografía simple
• Ecografía
• Ecografía
4) Evaluación de la formación de cápsula
• TC Ecografía
• Ecografía con contraste
• TC
• RM
• Ecografía con contraste
• TC
• RM
5) Diagnóstico de la obstrucción biliar, litiasis vesicular y diferenciación de quistes y lesiones hepáticas cólicas.
• Ecografía
• TC
• TC
6) Detección de lesiones hepáticas pequeñas (<5 mm.)
• Ecografía intraoperatoria
7) Evaluación del lóbulo izquierdo y los ganglios linfáticos del ligamento gastrohepático y, guiar la aspiración con aguja fina
• Ecografía endoscopia
8) para evaluar la permeabilidad de los grandes vasos y la hipertensión portal
• Ecografía Doppler
9) El estándar de oro para la detección y localización de las lesiones focales
• RM o
• TC helicoidal dinámica de triple fase (contraste de las fases venosa y arterial) (la
cuarta fase es la rastreo venoso retardado)
• TC helicoidal dinámica de triple fase (contraste de las fases venosa y arterial) (la
cuarta fase es la rastreo venoso retardado)
10) Diferenciación de las lesiones benignas de las malignas aunque no es muy útil para el HC
• TC FDG- PET (tomografía por emisión de positrones con FDG (18F-fludesoxiglucosa)
11) Diagnóstico de la hiperplasia nodular focal
• centellograma nuclear con Tc-99-sulfuro coloidal
12) Diagnóstico de tumores neuroendocrinos
• centellograma con MIBG (yodo-131-metayodobenzilguanidina y octreotida)
centellograma con octreotida
centellograma con octreotida
13) Diagnóstico de hemangiomas > 2,5 cm.
• Centellograma hepático con glóbulos rojos marcados con Tc-99 (la mayoría de los centros universitarios no utilizan este método y prefieren la ecografía con contraste, la TC y la RM).
Los agentes de contraste para la ecografía y la RM con hierro o gadolinio contrastan mejor para detectar las lesiones más pequeñas, las lesiones satélite o las metástasis a distancia.
Las características radiográficas del HC son: presencia de cápsula que supera el contorno hepático normal o una lesión con de densidad heterogénea. La inyección de contraste produce una marcación inmediata de la mayoría de los hematomas.
Punción aspiración con aguja fina (PAAF) y biopsia central (BC)
La PAAF y la BC son procedimientos seguros, eficaces y costo efectivos. Su especificidad es casi del 100% y su sensibilidad del 67-100%. Bajo la guía tomográfica o ecográfica, es el método de elección. La PAAF es superior a la BC pero son métodos complementarios con una certeza el 78% si se usan separados y del 88% si se complementan. Sin embargo, muchas patologías se diagnostican mejor mediante la BC que con la PAAF porque, por ejemplo, el HC bien diferenciado no puede ser separado del hígado normal.
Las complicaciones (en su mayoría hemorrágicas) son raras, con 0,5% de complicaciones menores y 0,05% de complicaciones mayores. Otro problema es la posibilidad de diseminación tumoral. La PAAF permite el diagnóstico en más del 50% de los casos, y llega al 65% cuando se realiza un segundo pasaje. Si se obtiene un bloque celular se consigue un diagnóstico tumoral adicional de 5-10%. Los criterios citológicos de Cohn ayudan a distinguir el HC de las lesiones no neoplásicas (81% de los HC cumplen al menos con 2 criterios).
Enfoque general para el manejo de los tumores hepáticos en hígados cirróticos
Tumores mayores de 2 cm.
El mejoramiento de la fase arterial y de lavado en la fase venosa portal es esencial para el diagnóstico de una lesión hepática >2 cm. en un hígado cirrótico. Más del 80% de los tumores >2 cm. en un hígado cirrótico son HC. Una AFP elevada confirma el diagnóstico. Si la AFP es normal, se recurrirá a las imágenes (TAC trifásica, RM). Si todavía hay dudas, podría estar indicada la PAAF-BC.
Tumores menores de 2 cm.
El 75% de los tumores <2 cm. en un hígado cirrótico son HC. Los niveles de AFP y las imágenes pueden garantizar el diagnóstico. Si aún hay dudas, se repite la imagen de la lesión pero ampliada, o podría estar indicada una PAAF/BC. Debido al riesgo de diseminación del tumor, si es posible una resección quirúrgica debe evitarse la biopsia. Un nódulo pequeño puede ser preneoplásico o benigno. La American Association for the Study of Liver Diseases (AASLD)distingue las lesiones <1 cm. de las >1 cm. pero <2 cm. Ellos sugieren realizar dos de las siguientes técnicas por imágenes : ecografía, TC y RM con contraste intravenoso.
Si mediante las dos técnicas se visualizan lesiones que cumplen los criterios preestablecidos, entonces es posible diagnosticar el HC. Los nódulos más grandes deben ser estudiados y los más pequeños supervisados cada 3 meses. Caturelli mostró que el 69% de los nódulos de novo en un hígado cirrótico es maligno. Por otra parte, la displasia de las células hepáticas se halla en el 60% de los hígados cirróticos con HC, y en sólo el 10% de los hígados no cirróticos.
Aumento de la AFP sin tumor hepático
En este caso, se debe repetir la TC o la RM dinámica cada 3 meses. Una AFP elevada no necesariamente es diagnóstica de HC, especialmente en los pacientes con el virus de la hepatitis C, quienes suelen tener una elevación leve de la AFP sin HC. Una AFP marcada es útil pero las elevaciones leves en ausencia de un tumor hepático no serían una indicación de trasplante hepático.
Hepatocarcinoma: es una enfermedad común, con una incidencia de 1%-6% en pacientes cirróticos. Los factores de riesgo son: cirrosis, ingesta de alcohol, virus de las hepatitis B y C, enfermedades metabólicas, carcinógenos ambientales, tratamientos hormonales y tabaquismo. El 90-95% de los HC aparecen en los hígados cirróticos. Los estudios de autopsias indican que el 20%-40% de los pacientes con cirrosis tienen HC. Tanto el tamaño como la gravedad de la enfermedad hepática influyen en la supervivencia. Los pacientes con tumores <5 cm. tienen una supervivencia del 80% en 1 año y del 20% a los 3 años.
Hepatocarcinoma: es una enfermedad común, con una incidencia de 1%-6% en pacientes cirróticos. Los factores de riesgo son: cirrosis, ingesta de alcohol, virus de las hepatitis B y C, enfermedades metabólicas, carcinógenos ambientales, tratamientos hormonales y tabaquismo. El 90-95% de los HC aparecen en los hígados cirróticos. Los estudios de autopsias indican que el 20%-40% de los pacientes con cirrosis tienen HC. Tanto el tamaño como la gravedad de la enfermedad hepática influyen en la supervivencia. Los pacientes con tumores <5 cm. tienen una supervivencia del 80% en 1 año y del 20% a los 3 años.
La aparición en un paciente cirrótico de un dolor abdominal nuevo, hepatomegalia reciente, hemoperitoneo, fiebre persistente o pérdida de peso debe hacer sospechar el HC. El Laboratorio que caracteriza al HC muestra un incremento repentino de la fosfatasa alcalina, un aumento de la relación AST/ALT, eritrocitosis, leucocitosis persistente, hipoglucemia recurrente, hipercolesterolemia e hipercalcemia. Los últimos cuatro resultados son manifestaciones paraneoplásicas, junto con el síndrome hormonal ectópico, la osteoartropatía hipertrófica y la porfiria cutanea tarda. Las complicaciones del HC incluyen la ictericia obstructiva y la ruptura del HC (60% -90% de mortalidad).
La detección del HC se hace mediante la ecografía más la determinación del nivel de AFP cada 6 meses. La guía de la AASLD solo recomienda la ecografía ya que consideran que la AFP es de poco valor adicional. Las lesiones >2 cm. solo necesitan de una técnica de imagen para detectar los signos (hipervascularización arterial) o una técnica de imagen más un nivel de AFP > 400, con el fin de hacer un diagnóstico no invasivo del HC. Las lesiones <2 cm. se dividen en mayores y menores de 1 cm. Los nódulos >1 cm. pero <2 cm. (1-2 cm.) requieren de un estudio diagnóstico con 2 o más técnicas por imágenes.
Los Nódulos <1 cm. necesitan exámenes de seguimiento cada 3 meses. El 9-37% de los HC son resecables en el momento del diagnóstico. Las contraindicaciones para la resección incluyen la cirrosis descompensada, las metástasis extrahepáticas, el compromiso de los ganglios hepática o de la vena cava inferior o, la expansión biliar. Las variantes histológicas en los hígados cirróticos son : trabecular (65%), mixta (15%), compacto (12%), seudoglandular (5%), fibrosis lamelar (1,5%) y escirro 0,5%.
Nódulos de regeneración: los nódulos displásicos se desarrollan a menudo dentro de los nódulos de regeneración cirróticos. Pueden mostrar displasia de alto o bajo grado. Es posible que los HC bien diferenciados y poco diferenciados se desarrollen por una progresión de la regeneración de los nódulos con displasia de bajo grado a una displasia de alto grado. La RM diferencia mejor las lesiones iso o hipointensa de los HC que las lesiones intensa o hiperintensas. En el más difícil de los casos, después de la resección hepática o del trasplante de hígado se hace necesaria la histología. Si no se puede confirmar la presencia de un HC se recomienda repetir la investigación más adelante. Con el tiempo, la displasia de alto grado de los nódulos puede convertirse en maligna, lo que sugiere la ablación preventivas mediante el etanol.
Enfoque general de los tumores hepáticos en el hígado no cirrótico
Los tumores hepáticos presentan fiebre, dolor abdominal, malestar o, en ocasiones, puede no tener sintomatología evidente. Los tumores benignos incluyen: hemangioma, hiperplasia nodular focal, hiperplasia nodular regenerativa (HNR) y el adenoma hepático. La mayoría de las neoplasias frecuentes son la gastrointestinal, la urogenital, el pulmón o las metástasis del carcinoma de mama. El cáncer primario de hígado incluye el carcinoma fibrolamelar, el colangiocarcinoma, el linfoma hepático y el angiosarcoma.
El diagnóstico de HC en un paciente con AFP elevada requiere estudios por imágenes. La ecografía o la TC clasifican los quistes, las metástasis y el hemangioma. La RM identifica el hígado graso focal la HNR, el adenoma hepático y el hemangioma. Cuando el diagnóstico sigue siendo incierto hay que considerar la PAAF o el seguimiento mediante imágenes. En los adnomas grades (> 5 o en crecimiento cm.) está indicada la resección.
Lesiones benignas
Hemangioma: Los hemangiomas se encuentran en el 20% de la población en general, siendo más frecuente en las mujeres. La mayoría son asintomáticos. Los hemangiomas gigantes (> 4 cm.) son sintomáticos en el 40% de los casos. Los síntomas son raros y pueden ser dolor abdominal, saciedad precoz, anorexia, náuseas. Para las lesiones >2,5 cm., el SPECT con glóbulos rojos marcados con Tc-99m es la técnica que mejor los y a menor costo (especificidad: 100%) mientras que para las lesiones <2 cm. es mejor la RM. Los centros universitarios rara vez recurren al SPECT con glóbulos rojos marcados para el diagnóstico de los hemangiomas debido a la utilización de la sección transversal de las imágenes.
La histología de los hemangiomas hepáticos muestra sinusoides vasculares llenos de sangre separados por paredes de tejido conectivo (peliosis: carece de la capa endotelial y de las trabéculas fibrosas). El riesgo de rotura es mínimo y no justifica la resección. Otras complicaciones son la trombosis, la esclerosis y la calcificación. Los hemangiomas hepáticos pueden crecer durante el embarazo o por los anticonceptivos orales. El síndrome de Kasabach-Merritt (coagulopatía de consumo) y de Bornman-Terblanche- Blumgart (fiebre y el síndrome de dolor abdominal), constituyen complicaciones poco frecuentes.
Hiperplasia nodular focal (HNF): es más frecuente en las mujeres de 20-50 años (80%). La patogenia es desconocida, pero incluye una lesión vascular. La lesión es generalmente <3 cm., asintomática y se descubre de forma accidental. La principal dificultad para el médico es diferenciarla de un adenoma o un carcinoma fibrolamelar en los estudios por imágenes. Sin embargo, los carcinomas fibrolamelar se intensifican y se lavan en forma heterogénea y presentan calcificaciones centrales y adenopatías. Estas características son muy raras en la HNF. La falta de síntomas, las enzimas hepáticas normales y el no uso de anticonceptivos orales argumentan en su favor.
La RM tiene un 70% de sensibilidad y una especificidad del 98% (lesión hipervascular homogénea con cicatriz central). Si la radiología no deja dudas, la mayoría de los hepatólogos abogan por una actitud expectante. De lo contrario, se hará una biopsia percutánea guiada por imágenes, para obtener tejido hepático tumoral y normal. La histología es similar a la de la cirrosis inactiva, con proliferación de hepatocitos en torno a una arteria central normal prominente con una cicatriz fibrosa central. La historia natural de la hiperplasia nodular focal es variable (estable, regresiva o progresiva en el tiempo), pero la resección no es necesaria debido a que no se maligniza. Las complicaciones son raras e incluyen trombosis de la vena hepática o el síndrome de Kasabach-Merritt.
Adenoma hepático: E adenoma se produce en las mujeres que toman anticonceptivos orales durante al menos 5 años o en pacientes diabéticos. Los adenomas múltiples están asociados con la enfermedad por almacenamiento de glucógeno tipo I y tipo Ⅲ. La adenomatosis (> 10 adenomas) se observa en pacientes que consumen esteroides anabólicos androgénicos. Es común el malestar abdominal.
Adenoma hepático: E adenoma se produce en las mujeres que toman anticonceptivos orales durante al menos 5 años o en pacientes diabéticos. Los adenomas múltiples están asociados con la enfermedad por almacenamiento de glucógeno tipo I y tipo Ⅲ. La adenomatosis (> 10 adenomas) se observa en pacientes que consumen esteroides anabólicos androgénicos. Es común el malestar abdominal.
En la ecografía, la lesión es hipoecoica o hiperecoica y en la TC es hipodensa o hiperdensa. La RM no es específica. Las lesiones son a menudo <8 cm. pero pueden ser >15 cm. Al microscopio aparecen como láminas homogéneas de hepatocitos normales o pequeños sin conducto biliar, tracto portal o vena central. El 5% de los adenomas hepáticos se transforma en HC. La inmunotinción con β-catenina podría ser útil para el diagnóstico. La rotura espontánea y el hemoperitoneo ocurren en el 10% de los casos, especialmente durante la menstruación, el embarazo o después del parto. La mayoría de los hepatólogos aboga por la resección y la interrupción de los anticonceptivos orales.
Hiperplasia nodular regenerativa y transformación nodular parcial (TNP)): la HNR (nódulos de regeneración grandes) está asociada con la enfermedad de Behcet, enfermedades reumáticas, trastornos mieloproliferativos, la congestión venosa crónica, los tumores neuroendocrinos metastásico, el síndrome de Budd-Chiari, y diversos medicamentos (esteroides, anticonceptivos, antineoplásicos, anticonvulsivos, e inmunosupresores). Las lesiones se presentan con hipertensión portal y colestasis. Rara vez se requiere el diagnóstico mediante la biopsia hepática abierta.
La HNR muestra un engrosamiento difuso con placas de células del hígado sin fibrosis en los nódulos hiperplásicos. Son características las alteraciones de la reticulita. La trombosis de la vena porta podría conducir a HNR por la atrofia del parénquima y la hiperplasia compensatoria. La trombosis de la vena porta también ha sido invocada en la patogenia de la TNP.
Infiltración grasa focal del hígado: en el 10% de los pacientes con hígado graso, la grasa se acumula focalmente o muestra focos en el segmento anteromedial del lóbulo izquierdo.. Estos pacientes generalmente tienen diabetes, hiperlipidemia, obesidad, son consumidores de alcohol o toman esteroides. En la ecografía la grasa de ve hiperecoica y en la TC tiene baja atenuación. El hígado graso focal no desplaza los vasos intrahepáticos. Las imágenes estándar de oro están dadas por la RM con aumento de la señal en la secuencia T1. las técnicas de supresión de la grasa también son muy prometedoras.
Otros tumores benignos raros
Cistoadenoma hepatobiliar: Esta lesión es poco frecuente, se presenta principalmente en mujeres de mediana edad y son causa de dolor abdominal. Se diferencia del quiste benigno por tener una pared gruesa septadas. Hasta el 25% son malignos (cistoadenocarcinoma), por lo tanto está indicada la extirpación quirúrgica.
Cistoadenoma hepatobiliar: Esta lesión es poco frecuente, se presenta principalmente en mujeres de mediana edad y son causa de dolor abdominal. Se diferencia del quiste benigno por tener una pared gruesa septadas. Hasta el 25% son malignos (cistoadenocarcinoma), por lo tanto está indicada la extirpación quirúrgica.
Adenomas de las vías biliares (colangioma): Los adenomas de las vías biliares son nódulos solitarios subcapsulares de 1-20 mm., descritos en pacientes con α-1-antitripsina. Los conductos biliares son más pequeños y no contienen bilis.
Papilomatosis biliar: Solo se han descrito 50 casos en todo el mundo. Es un tumor de la mediana edad que conduce a la obstrucción biliar por diseminación del tumor, moco, litiasis, colangitis y hemobilia. El diagnóstico se realiza por colangiopancreatografía retrógrada endoscópica (CPRE), la cual muestra la secreción mucinosa típico de
una ampolla dilatada, múltiples defectos de relleno y estenosis. La cura puede obtenerse mediante la hepatectomía
.
Tumores mesenquimático y nerviosos: esta categoría incluye lipomas, miolipomas, angiomiolipomas, schwannomas, neurofibromas y condromas.
una ampolla dilatada, múltiples defectos de relleno y estenosis. La cura puede obtenerse mediante la hepatectomía
.
Tumores mesenquimático y nerviosos: esta categoría incluye lipomas, miolipomas, angiomiolipomas, schwannomas, neurofibromas y condromas.
Seudotumor inflamatorio: Esta es afección inflamatoria de hombres rara, benigna,en hombres de mediana edad. Los pacientes pueden presentar fiebre, pérdida de peso, leucocitosis y elevación de la eritrosedimentación . Si la biopsia confirma el diagnóstico no sería necesaria de resección, sino que debería tratarse su origen.
Seudolesiones: se denomina seudolesión a una zona no patológica con una intensidad de señal diferente, atribuible a una alteración focal de la hemodinámica o el metabolismo parenquimatoso. Las seudolesiones observadas en los hígados cirróticos y no cirróticos incluyen cortocircuidos arterio-portales, nódulos de regeneración, fibrosis confluente y la afluencia anormal de sangre.
Lesiones malignas
Metástasis hepáticas: El hígado es el sitio más común de metástasis de neoplasias del tracto gastrointestinal, páncreas, mama y pulmón. Los defectos múltiples en las imágenes del hígado hacen sospechar un proceso metastásico. Sólo el 20% de los hígados presenta metástasis como una lesión solitaria. En general, están comprometidos ambos lóbulos hepáticos. En la TC, las metástasis colorrectales aparecen como lesiones de baja atenuación, a menudo con bordes irregulares y centro necrótico.
Durante la fase vascular precoz de la TC dinámica, las metástasis aparecen con una intensificación creciente. La sensibilidad de la TC (85%) puede aumentase con la TC-portografía arterial. La ecografía intraoperatoria posee una sensibilidad y especificidad excelentes para las metástasis del adenocarcinoma colorrectal. Una modalidad prometedora es la TC por emisión de positrones con FDG, el cual se acumula en las células con hipermetabolismo. Los cánceres de colon, pulmón y mama pueden ser estatificados mediante la CT con emisión de positrones con una sensibilidad del 92%-100% y una especificidad del 85%-100%. A menudo, la hipervascularidad de los tumores neuroendocrinos es evidente en la TC dinámica. La gammagrafía de los receptores de somatostatina puede localizar el 90% de los tumores neuroendocrinos (gastrinoma).
En el carcinoma colorrectal metastásico, el pronóstico mejora después de la resección quirúrgica. Las contraindicaciones de la resección son: número de metástasis hepáticas> 4, diseminación extrahepática y participación de los ganglios linfáticos hepáticos. Los tumores metastáticos del hígado calcificados podrían ser: leiomiosarcoma, sarcoma osteogénico, rabdomiosarcoma, condrosarcoma, cistoadenocarcinoma ovárico, melanoma, mesotelioma pleural, neuroblastoma y tumores testiculares. Las metástasis de estómago, páncreas, pulmón y mama calcificadas son extremadamente raras. La PAAF guiada ayuda a identificar la lesión primaria.
Hepatocarcinoma: casi todos los pacientes con el virus de la hepatitis C relacionado con el HC tienen cirrosis, mientras que los pacientes con HC relacionado con el virus de la hepatitis B son menos propensas a tener cirrosis. La ausencia de cirrosis hace que este tumor sea más pasibles de resección quirúrgica.
Carcinoma fibrolamelar: La variante fibrolamelar es un subtipo distintivo l HC pero no se asocia con los factores de riesgo clásicos de HC. Ocurre a una edad media de 26 años, se presenta como una gran masa solitaria, dolorosa que generalmente se encuentra en el lóbulo izquierdo. El nivel de AFP es normal. El término "fibrolamelar" se debe al aspecto microscópico de la lesión, con las capas delgadas de fibrosis que separa a los hepatocitos neoplásicos. En las imágenes puede verse una cicatriz fibrosa central. El 50% de las lesiones son resecables en el momento del diagnóstico.
Colangiocarcinoma intrahepático: representa el 20% de los tumores primarios del hígado y aparece como un adenocarcinoma o un carcinoma papilar o mucinoso. Los factores de riesgo son: cirrosis, colangitis esclerosante, adenoma de las vías biliares, quistes de colédoco, papilomatosis biliar, enfermedad de Carola y fasciola hepática. La ictericia es la presentación clínica más común. La presentación y el rápido aumento de la bilirrubina junto con la pérdida de peso despiertan la sospecha de colangiocarcinoma.
Los marcadores tumorales (CEA, CA-19-9 o AFP) podrían estar elevados. El CA 19-9 >100 tiene un 89% de sensibilidad y un 86% de especificidad de. Hay tres subtipos anatómicos: intrahepático periférico (15%,), perihiliar central (tumor de Klatskin) (60%) y, del conducto biliar distal común (25%). El colangiocarcinoma periférico se parece al HC sin cirrosis. Los tipos hiliar, central y distal se asocian con colangitis esclerosante, enfermedad inflamatoria intestinal u otras enfermedades biliares crónicas. La ecografía y la TC muestran una dilatación marcada del los conductos intrahepáticos. Un cambio brusco en el calibre del conducto biliar sugiere malignidad.
Para el diagnóstico del colangiocarcinoma se prefieren por su sensibilidad el análisis de las imágenes digitales y la hibridación fluorescente in situ, ya que son más sensibles que el cepillado estándar de rutina. La CPRE, la colangiografía percutánea transhepática y la RM permiten evaluar la resecabilidad.
La TC PET estatifica a estos tumores con una sensibilidad del 93%. El examen propuesto incluye ecografía, CEA y CA 19-9, cada 6 meses, Si hay estenosis biliar, están indicadas la CPRE y el cepillado. La combinación de HC y colangiocarcinoma muestra las características hepatocelulares y del epitelio biliar de ambos tumores.
Hemangioendotelioma epitelioide: Este cáncer de grado bajo afecta a individuos entre 20-80 años y se asocia con los anticonceptivos orales y la exposición al polivinilo. Se presenta con fiebre baja, dolor abdominal, hepatomegalia y enzimas hepáticas normales. Las células endoteliales se tiñen CD34, CD31 y Ⅷ factor. La resección quirúrgica o el trasplante hepático brindan un buen pronóstico.
Cistoadenocarcinoma: Generalmente aparece en el lóbulo derecho; es multiquístico y contiene material teñido de bilis. Se presenta con dolor abdominal y pérdida de peso. El pronóstico es bueno.
Linfomas y leucemia: La afectación hepática es común en la enfermedad de Hodgkin, incluyendo la infiltración linfomatosa (nódulos pequeños difusos o nódulos grandes), los fármacos, la hepatitis viral y la sepsis. La colestasis es poco común y se ha descrito el síndrome de evanescencia de los conductos biliares. El diagnóstico diferencial incluye los linfomas infiltrantes reactivos y los linfomas de células T.
El linfoma hepático primario es raro y puede presentarse como tumores solitarios o múltiples, como una lesión hepática difusa con hepatomegalia o como, insuficiencia hepática con LDH elevada. También se han descrito los linfomas de células T periférico gamma- delta con infiltración masiva sinusoidal hepática y del bazo. El hígado puede estar infiltrado en forma difusa o local por un mieloma múltiple o una leucemia (leucemia linfoide crónica, leucemia de células pilosas).
Tumores neuroendocrinos: Los tumores neuroendocrinos que se originan en el tracto gastrointestinal suelen dar metástasis en el hígado. Las metástasis hepáticas pueden ser resecadas. La quimioterapia tradicional no es eficaz, en cambio se ha comprobado respuesta al interferón-α. Los síntomas del síndrome carcinoide mejoran con los análogos de la somatostatina. El trasplante de hígado sigue siendo una opción.
Angiosarcoma: Se asocia con la exposición al cloruro de vinilo. La mayoría de los pacientes no son susceptibles de cirugía. Por lo general, están involucrado ambos lóbulos hepáticos y la tendencia a las metástasis contribuye a su mal pronóstico. La quimioterapia y la radioterapia no son útiles. La ligadura de de la arteria hepática sería un tratamiento paliativo.
Sarcoma indiferenciado de hígado: este tumor raro afecta principalmente a los niños. Las características clínicas son fiebre y un tumor hepático con hipoglucemia recurrente. La mediana de de la supervivencia es de 2 meses. Las imágenes muestran lesiones sólidas y quísticas con múltiples lóculos.
Otros tumores de células mesenquimáticas: el rabdomiosarcoma es el tumor más común de la vía biliar en los niños pequeños. El tumor puede simular un quiste del colédoco.
El fibrosarcoma se presenta como una masa hepática con hipoglucemia recurrente que se resuelve después de la resección. El interferón gamma -2 sérico está elevado. El leiomiosarcoma se presenta con deterioro general y dolor en el hipocondrio derecho. La angiografía TC muestra un tumor hipervascularizado. El trasplante hepático es posible.
El fibrosarcoma se presenta como una masa hepática con hipoglucemia recurrente que se resuelve después de la resección. El interferón gamma -2 sérico está elevado. El leiomiosarcoma se presenta con deterioro general y dolor en el hipocondrio derecho. La angiografía TC muestra un tumor hipervascularizado. El trasplante hepático es posible.
Biopsia de hígado versus resección del tumor hepático
Antes de la resección hepática, las lesiones deben ser medidas, contadas y localizadas en los segmentos de Couinaud. Se debe detallar su relación con las principales estructuras anatómicas (vena porta, arteria hepática, vena cava inferior y vena hepática). Si el cáncer es evidente, se recomienda evitar la biopsia debido a la posible diseminación. La histología del hígado obtenida por aguja cortante rinde más que la citología de la muestra por PAAF pero tiene varias desventajas. Si el tumor es pequeño (<3 cm.), el 20% de los casos requiere un segundo intento; se produce sangrado leve en el 1% de los casos se e intenso en el 0,1%. El 10% de los casos queda sin un diagnóstico de certeza, lo que indica la resección.
Antes de la resección hepática, las lesiones deben ser medidas, contadas y localizadas en los segmentos de Couinaud. Se debe detallar su relación con las principales estructuras anatómicas (vena porta, arteria hepática, vena cava inferior y vena hepática). Si el cáncer es evidente, se recomienda evitar la biopsia debido a la posible diseminación. La histología del hígado obtenida por aguja cortante rinde más que la citología de la muestra por PAAF pero tiene varias desventajas. Si el tumor es pequeño (<3 cm.), el 20% de los casos requiere un segundo intento; se produce sangrado leve en el 1% de los casos se e intenso en el 0,1%. El 10% de los casos queda sin un diagnóstico de certeza, lo que indica la resección.
El puntaje de Child Pugh ayuda a seleccionar los pacientes que deberán ser sometidos a la resección hepática. La supervivencia depende del potencial de regeneración y la presencia de cirrosis. Tradicionalmente, la cirrosis es una contraindicación de la resección hepática debido a la alta tasa de mortalidad (20%). Los pacientes con cirrosis que requieren una resección hepática plantean un dilema. El problema es que 10%-20% de los pacientes con cirrosis hepática tienen una neoplasia primaria. Además, el 80%-90% de los pacientes con HC y el 10%-20% de los pacientes con colangiocarcinoma tienen cirrosis. La mortalidad operatoria de resección amplia en pacientes sin cirrosis es del 10%.
Los diferentes tratamiento incluyen la ablación por radiofrecuencia, la inyección percutánea de etanol, la crioablación, la quimioembolización arterial hepática y la resección hepática laparoscópica. Los pacientes con cirrosis compensada podrían beneficiarse de la resección hepática, la ablación por radiofrecuencia o la quimioembolización de la arteria hepática, pero los pacientes con cirrosis descompensada es probable que no obtengan ningún beneficio en su supervivencia. En pacientes muy bien seleccionados con tumores incidentales, centrales o multifocales, el trasplante hepático podría ser más beneficioso.
Conclusión
Para el diagnóstico de los tumores hepáticos se analizan dos escenarios: (1) lesiones sólidas descubiertas incidentalmente en un paciente cirrótico. El diagnóstico más probable es el hepatocarcinoma, seguido por el nódulo displásico de alto y bajo grado. Lesiones >2 cm. se diagnostican por técnicas de imagen. Si las imágenes de las lesiones de 1-2 cm. son atípicas se debe recurrir a la histología.
Las lesiones <1 cm. requieren un seguimiento con ecografía cada 3 meses. (2) lesiones sólidas o tumores incidentales en un paciente no cirrótico. Las lesiones más frecuentes son el hemangioma, la hipertrofia nodular focal y el adenoma, los cuales deben ser descartados en mujeres jóvenes bajo tratamiento con anticonceptivos orales. Si la lesión se encuentra durante la estadificación o el seguimiento de un cáncer primario conocido y es de características dudosas se hace necesaria la histología. La mayoría de las metástasis hepáticas comunes provienen del adenocarcinoma de colon, estómago, pulmón, próstata o mama.
♦ Traducción y resumen objetivo: Dra. Marta Papponetti. Especialista en Medicina Interna
♦ Traducción y resumen objetivo: Dra. Marta Papponetti. Especialista en Medicina Interna
Suscribirse a:
Entradas (Atom)