Síndrome hepatorrenal en la cirrosis
Nuevas definiciones, criterios diagnósticos y recomendaciones terapéuticas surgidos del International Ascites Club que funcionó en la 59ª Reunión de la American Association for the Study of Liver Diseases.Autor: Dres. Francesco Salerno, Alexander Gerbes, Pere Gine` s, Florence Wong, Vicente Arroyo Fuente: Traducción y resumen objetivo: Dra. Marta Papponetti. Especialista en Medicina Interna. Gut 2007;56:1310–1318.
Desarrollo
El síndrome hepatorrenal (SHR) es una complicación grave de la enfermedad hepática terminal, el cual se presenta en pacientes con cirrosis avanzada y ascitis, quienes además presentan una disfunción circulatorio muy marcada; también aparece en pacientes con insuficiencia hepática aguda. A pesar de su naturaleza funcional, el SHR se asocia con mal pronóstico y el único tratamiento efectivo es el trasplante de hígado. Durante la 59ª Reunión de la American Association for the Study of Liver Diseases, el International Ascites Club funcionó un Grupo de Estudio sobre el SHR, con el propósito de informar los resultados de un taller internacional y llegar a un consenso sobre una nueva definición, y criterios diagnósticos y recomendaciones terapéuticas actualizados. Un taller similar se hizo en Chicago en 1994, en el cual es estandarizó la nomenclatura y los criterios diagnósticos para la ascitis refractaria y el SHR. La introducción de tratamientos innovadores y el mayor conocimiento de la patogénesis del SHR durante las últimas décadas generaron la necesidad de llegar a un nuevo consenso. Este estudio informa las razones científicas que generaron nuevas definiciones y recomendaciones.
El taller internacional incluyó cuatro temas debatidos por cuatro paneles de especialistas:
1) patogénesis del SHR basado en la evidencia,
2) tratamiento del SHR con vasoconstrictores,
3) otros tratamientos del SHR con colocación de stent y shunt portosistémicos intrahepáticos transyugular (SPIT) y la diálisis extracorpórea de albúmina y,
4) nuevas definiciones, criterios diagnósticos y recomendaciones para el SHR.
Antecedentes
La definición y los criterios diagnósticos del SHR establecidos en 1994 se basaron en los 3 conceptos siguientes:
1) En el SHR, la insuficiencia renal es funcional y está causada por una intensa vasoconstricción arteriolar intrarrenal.
2) El SHR ocurre en pacientes con disfunción circulatoria sistémica causada por una vasodilatación extrarrenal.
3) La expansión del volumen plasmático no mejora la insuficiencia renal.
A partir de estos conceptos, surgieron otros nuevos:
a) La vasodilatación arterial extrarrenal ocurre principalmente en el lecho vascular esplácnico, mientras que otros lechos arteriales, como los que irrigan el cerebro y el hígado pueden estar vasocontraídos. Esto favorece el desarrollo de la encefalopatía cerebral y la insuficiencia cardíaca, respectivamente.
b) El gasto cardíaco en pacientes con SHR puede ser bajo, normal o elevado, pero es insuficiente para la necesidad del pacientes debido a las Resistencia periféricas reducidas.
c) El desencadenante más común para el desarrollo del SHR tipo 1 es la infección bacteriana, principalmente la peritonitis bacteriana espontánea (PBE).
d) La función renal puede mejorarse mediante el tratamiento médico en pacientes con SHR, lo cual mejora la supervivencia.
Antecedentes de los nuevos conceptos
El primero de esos conceptos fue formulado sobre la base de la investigación con ecografía Doppler o pletismografía, antes y después de 1994. Esos estudios fueron realizados en pacientes con cirrosis de diferente gravedad y mostraron la existencia de vasodilatación arterial en la circulación esplácnica como así vasoconstricción arterial en áreas como el cerebro, riñones e hígado, mientras que el flujo sanguíneo cutáneo y muscular fue informado como bajo, normal o aumentado. La dilatación de los vasos esplácnicos está causada sobre todo por la liberación local de vasodilatadores potentes como el óxido nítrico, el cual también favorece la resistencia de la circulación esplácnica a varios vasopresores como la angiotensina II, la noradrenalina, la vasopresina y la endotelina. Esta resistencia hace que la presión arterial en la cirrosis dependa de los efectos extraesplácnicos ejercidos por los vasoconstrictores endógenos. Como la vasodilatación arterial aumenta con la progresión de la cirrosis, el papel de los vasoconstrictores en mantener la estabilidad hemodinámica se torna crítico, y explica porqué los pacientes cirróticos con SHR están predispuestos a la vasoconstricción renal, hepática y cerebral.
El segundo concepto nuevo se trata del gasto cardíaco insuficiente en esos pacientes, el cual favorece la hipoperfusión renal, como ha sido confirmado recientemente. Entre los pacientes con SHR, la progresión de la disfunción circulatoria que llevó a la hipotensión arterial y a la insuficiencia renal se presentó en el grupo que desarrolló un descenso continuado del gasto cardíaco con aumento de la actividad de la renina plasmática. Estos hallazgos, dicen los autores, avalan la hipótesis que para mantener el volumen sanguíneo central y la perfusión renal en la cirrosis es muy importante contar con una circulación hiperdinámica. Por lo tanto, agregan, cuando el gasto cardíaco disminuye, aparece la hipovolemia, la hipoperfusión renal y el SHR. Se desconoce el mecanismo por el cual, en los pacientes con SHR, el gasto cardíaco se altera o se hace insuficiente.
Recientemente se ha identificado una anormalidad cardiaca específica, caracterizada por una menor respuesta sistólica y diastólica a los estímulos, cambios en la repolarización e hipertrofia de las cavidades cardíacas, denominada “miocardiopatía cirrótica”. Otra hipótesis es la existencia de una disminución del retorno venoso, lo que podría justificar la efectividad de la infusión de albúmina.
El SHR puede desencadenarse por eventos precipitantes. Los más importantes son la infección, la hemorragia y la paracentesis de grandes volúmenes sin la administración de albúmina. En la actualidad se le da mucha importancia al papel de la PBE.
Dos estudios que evaluaron la prevalencia de insuficiencia renal en pacientes cirróticos con PBE y en pacientes con infecciones no relacionadas con la PBE han comprobado que:
a) a pesar de un tratamiento antibiótico efectivo, una proporción importante de pacientes cirróticos con infección bacteriana desarrollaron una insuficiencia renal progresiva. Esto ocurre casi exclusivamente en pacientes con PBE
b) en los pacientes que no responden al tratamiento antibiótico, se presenta una insuficiencia renal progresiva independiente del tipo de infección. Por otra parte, las modificaciones de la función circulatoria, los sistemas vasoactivos endógenos y la función renal en pacientes que desarrollan insuficiencia renal desencadenada por la PBE son idénticas a las observadas en pacientes con SHR no relacionado con infección, lo que indica que la patogénesis de la insuficiencia renal progresiva en los cirróticos con infección es la misma que la del SHR.
Sin embargo, el concepto más importante del SHR surge de los estudios sobre nuevas estrategias terapéuticas. Dado que el SHR tipo 1 se asocia con un deterioro rápido de la función hepática con aumento de la bilirrubinemia y del tiempo de protrombina, se lo ha interpretado como una manifestación de la insuficiencia hepática terminal. El hecho que el SHR tipo 1 puede mejorarse mediante el uso de vasoconstrictores o por el SPIT y a que la regresión del SHR puede asociarse con mayor supervivencia, “representa un cambio importante en nuestro conocimiento del síndrome.”
En conclusión, los autores afirman que el principal mecanismo patogenético en el SHR tipo 1 es un deterioro potencialmente reversible de la función circulatoria sistémica, sobre todo debido a la vasodilatación esplácnica y a la vasoconstricción renal, con frecuencia desencadenadas por un factor precipitante. Además de la insuficiencia renal, el síndrome puede asociarse con otras disfunciones orgánicas, como el descenso del gasto cardíaco, la insuficiencia renal y la encefalopatía.
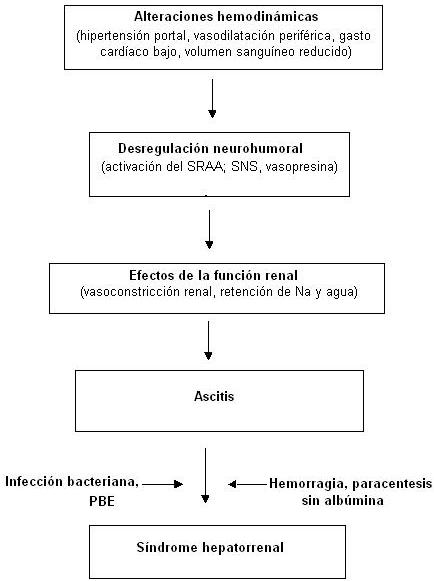
SRAA: sistema renina-angiontensina-aldosterona; PBE: peritonitis bacteria espontánea
Tratamiento del síndrome hepatorrenal
Se han desarrollado nuevos tratamiento del SHR para expandir el volumen sanguíneo cerebral aumentando al mismo tiempo el volumen plasmático y reduciendo la intensa vasodilatación periférica. Los autores sostienen que esta estrategia no es enteramente nueva, ya que en 1967, Tristani y Cohn demostraron que la infusión de dextrano mejoraba el gasto cardíaco y la perfusión renal en los pacientes cirróticos oligúricos. Dieciocho años después, Shapiro y col. demostraron que, en los pacientes cirróticos con ascitis, la excreción de agua y sodio por orina mejoraba con la administración de noradrenalina y las maniobras destinadas a expandir el volumen sanguíneo central (inmersión en agua). Sin embargo, los resultados de importancia clínica solo se han obtenido recientemente con el uso de albúmina y vasoconstrictores. El mecanismo por el cual los vasoconstrictores y la albúmina mejoran el índice de filtración glomerular (IFG) en pacientes con SHR no se conoce bien. Sin embargo, la administración de terlipresina a pacientes con SHR aumenta la presión sanguínea y provoca un descenso importante de la actividad de la renina plasmática, y un aumento del IFG, lo que en forma indirecta indica que se produce una corrección de la disfunción circulatoria.
Es posible que los análogos de la vasopresina provoquen vasoconstricción del lecho esplácnico, permitiendo así la redistribución del volumen sanguíneo a ciertos órganos extraesplácnicos, incluyendo el compartimiento central y los riñones. El relleno del compartimiento central provoca la inhibición de los sistemas nervioso simpático y renina angiotensina, inclinando la curva autorreguladora hacia la izquierda y haciendo que el flujo sanguíneo renal y el IFG respondan más a las modificaciones de la presión arterial. Tradicionalmente, la albúmina siempre ha sido considerada un recurso para mejorar la función circulatoria en la cirrosis, a través de la expansión del volumen sanguíneo central y el aumento del gasto cardíaco. En general, los últimos estudios han demostrado que la administración de albúmina a pacientes cirróticos con PBE causa vasoconstricción arterial e hipertensión arterial, probablemente por la capacidad de la albúmina de unirse a los vasodilatadores. Por lo tanto, expresan los autores, es posible que una mejoría de la función renal en los pacientes con SHR tratados con vasoconstrictores y albúmina se deba a los efectos sumados que tienen los dos compuestos sobre la circulación arterial periférica.
Profilaxis del síndrome hepatorrenal
Basados en los resultados de algunos estudios, los autores sostienen que la profilaxis con albúmina debería quedar restringida a los pacientes con SHR tipo 1 y PBE, pero se requieren estudios para definir mejor la dosis óptima.
Vasoconstrictores y albúmina
Hace ya 35 años se propuso el uso de un análogo de la vasopresina para mejorar el flujo sanguíneo renal en los pacientes cirróticos. Se ha comprobado que la infusión de ornipresina mejora moderadamente el IFG, pero el fármaco fue infundido solo 4 horas, lo que no permitió la evaluación de los efectos a largo plazo. Otros dos estudios demostraron que la administración prolongada (1 a 2 semanas) de ornipresina combinada con albúmina o dopamina, normalizó la creatininemia en muchos pacientes con SHR de tipo 1. Es de destacar que la recurrencia de la insuficiencia renal solo ocurrió después de la suspensión del tratamiento, y en los pocos casos en los que se reinstaló un segundo curso terapéutico, el resultado fue exitoso. Sin embargo, dicen, el efecto adverso más frecuente de la ornipresina fue la complicación isquémica.
Por lo tanto, la difusión del uso clínico de los vasoconstrictores en pacientes con SHR solo tuvo lugar con el advenimiento de compuestos más seguros como la terlipresina, un análogo de la vasopresina con actividad más prolongada, y el agonista α2 midodrina combinado con octreotida. Los estudios sobre el uso de terlipresina muestran que:
a) aunque el IFG raramente alcanza niveles normales, un período corto de tratamiento con terlipresina mejora la función renal hasta en el 65% de los pacientes con SHR tipo 1
b) es probable que la efectividad de la terlipresina aumente con la albúmina
c) en casi el 20% de los pacientes, el SHR ocurre luego de la suspensión del tratamiento, pero su reinstauración suele ser efectiva
d) en la mayoría de los casos, la hiponatremia por dilución asociada con el SHR mejora con el tratamiento con terlipresina
e) los efectos colaterales graves del tratamiento no son comunes (5-10%).
Con respecto a la supervivencia, los pacientes que se recuperaron por completo de su SHR tipo 1 por efecto de la terlipresina tienen una mejoría de la supervivencia en el corto plazo, aunque otros estudios comprobaron que las supervivencias a los 60 días del seguimiento de pacientes tratados con terlipresina más albúmina y los tratados solo con albúmina eran iguales. Por lo tanto, faltan estudios sobre la supervivencia a largo plazo. Sin embargo, el uso de terlipresina para mejorar la función renal es un recurso de apoyo importante para los pacientes con SHR tipo 1 incluidos en listas de espera para trasplante hepático. En muchos trabajos, la dosis de terlipresina oscila entre 0,5 y 1 mg/4-6 horas. Este régimen se mantuvo hasta la reversión del SHR, la cual ocurrió hacia la segunda semana de tratamiento. En otros estudios, la dosis inicial para pacientes sin una respuesta rápida fue 2 mg/4-6 horas. La dosis diaria de albúmina fue de 20 a 40 g, precedida en algunos estudios por una carga de 1g/kg de peso corporal. Algunos consideran la presión venosa central para establecer y titular las dosis de albúmina y prevenir la sobrecarga líquida.
La experiencia con midodrina es más limitada. Hasta el momento, solo hubo dos estudios piloto en los que se uso la midodrina combinada con octreotida para mejorar el efecto de la vasoconstricción esplácnica, pero las dosis y las vías de administración fueron bastante diferentes. Dado que la octreotida sola no influye sobre el IFG en los pacientes con SHR, se deduce que la acción más importante sobre el IFG proviene de la
midodrina.
Un estudio piloto estudió la acción de una infusión de noradrenalina combinada con albúmina y furosemida con buenos resultados. La noradrenalina es más barata y disponible que la terlipresina, pero se cree que tiene mayor tendencia a inducir arritmias cardíacas. Por lo tanto, el papel de la noradrenalina en pacientes con SHR tipo 1 requiere más estudios, sobre todo comparativos con la terlipresina o la combinación de midrodrina y octreotida.
El efecto del SPIT ha sido poco estudiado en el SHR. De los trabajos consultados, surge que:
a) en la mayoría de los pacientes con SHR tipo 1, después del SPIT se nota una supresión pronunciada de los sistemas vasoactivos endógenos, en particular del sistema renina angiotensina, y un descenso de los niveles de creatinina. El descenso de la creatinina fue más lento que cuando se utiliza terlipresina más albúmina.
b) la recurrencia del SHR fue rara, siempre que el shunt funcionara bien.
c) la encefalopatía hepática fue una complicación frecuente del SPIT pero fue manejada adecuadamente con tratamiento médico.
d) el SPIT casi siempre indujo una reducción del volumen de la ascitis.
e) la resolución del SHR tipo 1 por el SPIT puede mejorar la supervivencia.
f) el tratamiento secuencial con vasoconstrictores y albúmina seguido de SPIT podría utilizarse como un tratamiento alternativo para aumentar la probabilidad de beneficios a largo plazo.
g) aunque el SPIT puede mejorar la función renal y la ascitis refractaria en pacientes con SHR tipo 2, su efecto sobre la supervivencia todavía no ha quedado establecido.
Sin embargo, dado que casi todos los estudios excluyeron a los pacientes con antecedentes de encefalopatía grave, bilirrubinemia > 5 mg/dL, o un puntaje de Chile-Pugh >12, la aplicabilidad del SPIT puede ser más que limitada en los pacientes con SHR, quienes frecuentemente presentan ictericia, encefalopatía y puntaje elevado de Chile-Pugh. Existe poca investigación sobre el mecanismo por el cual el SPIT ejerce efectos beneficiosos en pacientes con SHR. Sin embargo, como el SPIT funciona como un shunt portocava látero-lateral, se espera que alivie la hipertensión portal, la cual representa un papel importante en la patogénesis de la vasodilatación arterial esplácnica. En general, el SPIT se asocia con mayor gasto cardíaco y la expansión del volumen sanguíneo central.
Diálisis de albúmina extracorpórea
Este procedimiento utiliza un líquido de diálisis con albúmina, libre de células, que es recirculado y prefundido a través de carbón y columnas de intercambios aniónico. El sistema también está conectado a un aparato de hemodiálisis o de hemoperfusión. De este modo se pueden eliminar sustancias unidas a la albúmina, como la bilirrubina, los ácidos biliares, los aminoácidos aromáticos, los ácidos grasos de cadena mediana y las citocinas. Hay pocos datos sobre la aplicación de este método en pacientes con SHR, y los mismos son controvertidos. Es un método muy costoso y todavía debe ser considerado experimental.
Trasplante de hígado en pacientes con síndrome hepatorrenal
El trasplante hepático fue el único tratamiento efectivo para los pacientes con SHR antes de la introducción de los vasoconstrictores y el SPIT, siendo todavía el tratamiento de elección para esos pacientes. Inmediatamente después del trasplante puede haber un empeoramiento del IFG y muchos pacientes requieren diálisis por muchos tiempo (35% de los pacientes trasplantados con SHR vs 5% de los pacientes trasplantados sin SHR). Los inhibidores de la calcineurina (ciclosporina y tacrolimus) pueden contribuir al empeoramiento del IFG. Luego, el IFG comienza a mejorar hasta alcanzar valores de 30 a 40 mL/min, 1 a 2 meses después de la operación. Esta insuficiencia renal moderada persiste durante el seguimiento y probablemente se deba a un mayor efecto nefrotóxico de los inhibidores de la calcineurina en pacientes con deterioro renal pretrasplante. En efecto, expresan los autores, las anormalidades hemodinámicas y neurohormonales asociadas con el SHR desaparecen en los primeros meses postrasplante y los pacientes recuperan su capacidad para excretar sodio y agua libre. Los pacientes con SHR que han recibido un trasplante hepático tienden a tener más complicaciones, estar más tiempo internados en Terapia Intensiva y mayores tasas de mortalidad intrahospitalaria que los pacientes con trasplante hepático sin SHR. No obstante, su supervivencia a los 3 años es aceptable (60% vs 70-80 en pacientes trasplantados hepáticos sin SHR).
La principal limitación del trasplante hepático es que debido a la escasez de donantes de órganos, y su extremadamente corta supervivencia, la mayoría de los pacientes con SHR tipo 1 muere antes del trasplante. La introducción del modelo de enfermedad hepática terminal para priorizar el órgano a ser trasplantado ha solucionado en parte este problema, ya que los pacientes con SHR tienen una alta prioridad en las listas de espera. Por otra parte, el tratamiento con vasoconstrictores y albúmina del SHR tipo 1 puede mejorar la supervivencia del paciente y, por lo tanto, mejorar su probabilidad de ser trasplantado.
1314
El mayor conocimiento de los mecanismos que subyacen el SHR y el desarrollo de estrategias terapéuticas nuevas son las razones para el nuevo consenso sobre la definición, criterios diagnósticos y tratamiento del SHR organizado por el International Ascites Club.
Nuevas definiciones del síndrome hepatorrenal
El SHR es un síndrome potencialmente reversible que ocurre en pacientes con cirrosis, ascitis e insuficiencia hepática, como así en pacientes con insuficiencia hepática aguda o hepatitis alcohólica. Se caracteriza por deterioro de la función renal, alteraciones marcadas de la función cardiovascular e hiperactividad de los sistemas nervioso simpático y renina angiotensina. La vasoconstricción renal intensa provoca un descenso del IFG. Existen dos tipos de SHR. El SHR de tipo 2 se caracteriza por una insuficiencia renal moderada (creatininemia 1,5 a 2,5 mg/dL), con un curso estable o lentamente progresivo. Aparece en forma espontánea pero también por un evento precipitante. El tipo 2 se asocia generalmente con ascitis refractaria. La supervivencia de los pacientes de este grupo es más corta que la de los cirróticos no urémicos con ascitis, pero mejor que la de los pacientes con SHR tipo 1.
El SHR de tipo 1 se caracteriza por insuficiencia renal rápidamente progresiva definida por la duplicación de las concentraciones de creatinina sérica hasta un nivel mayor a 2,5 mg/dL, en menos de 2 semanas. Aparece en forma espontánea, pero suele desarrollarse luego de un evento precipitante, en particular la PBE. Suele ocurrir en el contexto de un deterioro agudo de la función circulatoria, caracterizado por hipotensión arterial y activación de los sistemas vasoconstrictores endógenos. Puede asociarse con insuficiencia cardíaca y hepática como así con encefalopatía. El pronóstico del tipo 1 es muy malo. Las diferencias principales con la definición de 1996 son:
a) la potencial reversibilidad del SHR sin trasplante hepático;
b) el papel dominante del lecho esplácnico en la vasodilatación arterial;
c) la participación frecuente de la PBE como un evento precipitante en el SHR tipo 1;
d) el concepto de que, además de la insuficiencia renal, es frecuente la insuficiencia concomitante de otros órganos, en particular el corazón;
Criterios diagnósticos revisados del síndrome hepatorrenal
Debido a que no existen características especificas del SHR, el diagnóstico se basa en la exclusión de otros tipos de insuficiencia renal. Los criterios necesarios para diagnosticar el SHR son los siguientes:
Las principales diferencias entre esos criterios y los establecidos con anterioridad son:
a) el clearance de creatinina ha sido excluido por que es más complicado en la práctica que el uso de la creatininemia simple y no aumenta la precisión del cálculo de la función renal en los pacientes cirróticos.
b) en la actualidad, se considera SHR a la insuficiencia renal en presencia de infección bacteriana pero en ausencia de shock séptico. Esto significa que el tratamiento del SHR debe iniciarse sin esperar a la recuperación completa de la infección.
c) la expansión del volumen plasmático debe realizarse con albúmina más que con solución salina.
d) se han eliminado los criterios diagnósticos menores por no ser esenciales.
Tratamiento del síndrome hepatorrenal
La mayoría de los datos disponibles hasta el momento sobre el tratamiento del SHR provienen de análisis retrospectivos, estudios piloto, estudios comparativos no aleatorizados y solo uno pocos trabajos controlados y aleatorizados. Por otra parte, la mayoría de los estudios han incluido demasiado pocos pacientes. Por lo tanto, aclaran los autores, los conceptos y las recomendaciones prácticas que aparecen en esta parte del artículo están basados en datos publicados y en la experiencia personal de los panelistas, y puede ser mejorada a medida que se acumule más experiencia.
Prevención del síndrome hepatorrenal
La incidencia del SHR en pacientes con PBE puede reducirse con la administración de albúmina, prevención ésta que se asocia con un alargamiento de la supervivencia. La dosis de albúmina sugerida es de 1,5 g/kg de peso corporal, el primer día, seguido en el tercer día por 1 g/kg de peso corporal, hasta un máximo de 150 a 100 g, respectivamente. La administración de albúmina está indicada en los pacientes con PBE y bilirrubinemia (4 mg/día) o creatinina sérica (> 1 mg/dL). Se requieren más estudios para determinar la dosis óptima de albúmina y al subgrupo de pacientes en quienes el tratamiento está muy indicado.
Tratamientos efectivos del síndrome hepatorrenal
Trasplante de hígado
Éste es el tratamiento de elección para ambos tipos de SHR. La morbilidad luego del trasplante hepático es superior en los pacientes con SHR que en los pacientes sin SHR, aunque la probabilidad a largo plazo de supervivencia es solo algo menor. La inversión del SHR tipo 1 mediante el tratamiento farmacológico antes del trasplante hepático puede mejorar la supervivencia después del trasplante. La reducción de la creatinina sérica luego del tratamiento y la disminución relacionada del puntaje de la hepatopatía no cambia la decisión de realizar el trasplante hepático, ya que el pronóstico luego de la recuperación del SHR tipo sigue siendo muy malo.
Tratamiento farmacológico con vasoconstrictores
Los estudios sobre el tratamiento farmacológico del SHR se han realizado principalmente en pacientes con SHR tipo 1, siendo la terlipresina es el compuesto más estudiado. Su dosis inicial es de 1 mg/4-6 horas, y si no hay respuesta (>25% de disminución de la creatininemia luego de 2 días), se puede duplicar la dosis cada 2 días, hasta un máximo de 12 mg/día. El tratamiento puede detenerse cuando la creatinina sérica no disminuye al menos 50% luego de 7 días de la dosis máxima o, si no se produce el descenso luego de los primeros 3 días. En los pacientes con respuesta inmediata, el tratamiento debe continuarse hasta la reversión del SHR o hasta un efecto máximo de 14 días. La terlipresina puede inducir isquemia y arritmias lo que obliga a suspender su aplicación. Otros vasoconstrictores son la midodrina o la noradrenalina.
Para adaptar las dosis de vasoconstrictores, además de la creatininemia se pueden utilizar la presión arterial, la excreción renal de agua y sodio y la natremia. La administración de albúmina puede mejorar el efecto de los vasoconstrictores. La albúmina se debe suspender cuando su concentración sérica supera los 45 g/L o en presencia de edema pulmonar.
En respuesta al tratamiento con vasoconstrictores y albúmina se pueden esperar tres tipos de respuesta: la respuesta completa ocurra en el 60% de los pacientes tratados con terlipresina, pudiendo mejorar la supervivencia. Puede haber una recaída de la insuficiencia renal puede luego de la suspensión del tratamiento pero un nuevo tratamiento suele ser efectivo. Por el contrario, la respuesta parcial a menudo es seguida por una recaída grave e irreversible de la insuficiencia renal.
Stent-shunt portosistémicos intrahepáticoa transyugular
Los pocos datos existentes sobre los resultados del SPIT en el SHR muestran que mejora la función renal y elimina la ascitis. En los pacientes con SHR tipo 1, el SPIT puede mejorar la supervivencia pero es su resultado es dudoso en el SHR tipo 2. La mayor desventaja del SPIT es su baja aplicabilidad ya que puede usarse en pacientes con bilirrubinemias mayores de 5 mg/dL, encefalopatía grave o el antecedente de encefalopatía recurrente, infección bacteriana grave, disfunción cardíaca o pulmonar grave o puntaje de Chile-Pugh >11.
Recomendaciones finales para el tratamiento de los pacientes con síndrome hepatorrenal
SHR tipo 1
El tratamiento de primera línea es el uso de vasoconstrictores combinados con albúmina. Los pacientes que no responden a los vasoconstrictores o lo hacen parcialmente pueden ser tratados con SPIT. Si hay contraindicaciones para el SPIT, se puede recurrir a la diálisis de albúmina extracorpórea, en el contexto de estudios prospectivos.
El uso secuencial de vasoconstrictores más albúmina y SPIT en pacientes elegibles es una idea interesante para proseguir las investigaciones.
SHR tipo 2
No hay datos definitivos que avalen el uso de vasoconstrictores en estos pacientes., El SPIT puede usarse para mejorar la ascitis refractaria, la cual es frecuente en el SHR tipo 2. Poco se sabe sobre el efecto del SPIT sobre la supervivencia a largo plazo.
El taller internacional incluyó cuatro temas debatidos por cuatro paneles de especialistas:
1) patogénesis del SHR basado en la evidencia,
2) tratamiento del SHR con vasoconstrictores,
3) otros tratamientos del SHR con colocación de stent y shunt portosistémicos intrahepáticos transyugular (SPIT) y la diálisis extracorpórea de albúmina y,
4) nuevas definiciones, criterios diagnósticos y recomendaciones para el SHR.
Antecedentes
La definición y los criterios diagnósticos del SHR establecidos en 1994 se basaron en los 3 conceptos siguientes:
1) En el SHR, la insuficiencia renal es funcional y está causada por una intensa vasoconstricción arteriolar intrarrenal.
2) El SHR ocurre en pacientes con disfunción circulatoria sistémica causada por una vasodilatación extrarrenal.
3) La expansión del volumen plasmático no mejora la insuficiencia renal.
A partir de estos conceptos, surgieron otros nuevos:
a) La vasodilatación arterial extrarrenal ocurre principalmente en el lecho vascular esplácnico, mientras que otros lechos arteriales, como los que irrigan el cerebro y el hígado pueden estar vasocontraídos. Esto favorece el desarrollo de la encefalopatía cerebral y la insuficiencia cardíaca, respectivamente.
b) El gasto cardíaco en pacientes con SHR puede ser bajo, normal o elevado, pero es insuficiente para la necesidad del pacientes debido a las Resistencia periféricas reducidas.
c) El desencadenante más común para el desarrollo del SHR tipo 1 es la infección bacteriana, principalmente la peritonitis bacteriana espontánea (PBE).
d) La función renal puede mejorarse mediante el tratamiento médico en pacientes con SHR, lo cual mejora la supervivencia.
Antecedentes de los nuevos conceptos
El primero de esos conceptos fue formulado sobre la base de la investigación con ecografía Doppler o pletismografía, antes y después de 1994. Esos estudios fueron realizados en pacientes con cirrosis de diferente gravedad y mostraron la existencia de vasodilatación arterial en la circulación esplácnica como así vasoconstricción arterial en áreas como el cerebro, riñones e hígado, mientras que el flujo sanguíneo cutáneo y muscular fue informado como bajo, normal o aumentado. La dilatación de los vasos esplácnicos está causada sobre todo por la liberación local de vasodilatadores potentes como el óxido nítrico, el cual también favorece la resistencia de la circulación esplácnica a varios vasopresores como la angiotensina II, la noradrenalina, la vasopresina y la endotelina. Esta resistencia hace que la presión arterial en la cirrosis dependa de los efectos extraesplácnicos ejercidos por los vasoconstrictores endógenos. Como la vasodilatación arterial aumenta con la progresión de la cirrosis, el papel de los vasoconstrictores en mantener la estabilidad hemodinámica se torna crítico, y explica porqué los pacientes cirróticos con SHR están predispuestos a la vasoconstricción renal, hepática y cerebral.
El segundo concepto nuevo se trata del gasto cardíaco insuficiente en esos pacientes, el cual favorece la hipoperfusión renal, como ha sido confirmado recientemente. Entre los pacientes con SHR, la progresión de la disfunción circulatoria que llevó a la hipotensión arterial y a la insuficiencia renal se presentó en el grupo que desarrolló un descenso continuado del gasto cardíaco con aumento de la actividad de la renina plasmática. Estos hallazgos, dicen los autores, avalan la hipótesis que para mantener el volumen sanguíneo central y la perfusión renal en la cirrosis es muy importante contar con una circulación hiperdinámica. Por lo tanto, agregan, cuando el gasto cardíaco disminuye, aparece la hipovolemia, la hipoperfusión renal y el SHR. Se desconoce el mecanismo por el cual, en los pacientes con SHR, el gasto cardíaco se altera o se hace insuficiente.
Recientemente se ha identificado una anormalidad cardiaca específica, caracterizada por una menor respuesta sistólica y diastólica a los estímulos, cambios en la repolarización e hipertrofia de las cavidades cardíacas, denominada “miocardiopatía cirrótica”. Otra hipótesis es la existencia de una disminución del retorno venoso, lo que podría justificar la efectividad de la infusión de albúmina.
El SHR puede desencadenarse por eventos precipitantes. Los más importantes son la infección, la hemorragia y la paracentesis de grandes volúmenes sin la administración de albúmina. En la actualidad se le da mucha importancia al papel de la PBE.
Dos estudios que evaluaron la prevalencia de insuficiencia renal en pacientes cirróticos con PBE y en pacientes con infecciones no relacionadas con la PBE han comprobado que:
a) a pesar de un tratamiento antibiótico efectivo, una proporción importante de pacientes cirróticos con infección bacteriana desarrollaron una insuficiencia renal progresiva. Esto ocurre casi exclusivamente en pacientes con PBE
b) en los pacientes que no responden al tratamiento antibiótico, se presenta una insuficiencia renal progresiva independiente del tipo de infección. Por otra parte, las modificaciones de la función circulatoria, los sistemas vasoactivos endógenos y la función renal en pacientes que desarrollan insuficiencia renal desencadenada por la PBE son idénticas a las observadas en pacientes con SHR no relacionado con infección, lo que indica que la patogénesis de la insuficiencia renal progresiva en los cirróticos con infección es la misma que la del SHR.
Sin embargo, el concepto más importante del SHR surge de los estudios sobre nuevas estrategias terapéuticas. Dado que el SHR tipo 1 se asocia con un deterioro rápido de la función hepática con aumento de la bilirrubinemia y del tiempo de protrombina, se lo ha interpretado como una manifestación de la insuficiencia hepática terminal. El hecho que el SHR tipo 1 puede mejorarse mediante el uso de vasoconstrictores o por el SPIT y a que la regresión del SHR puede asociarse con mayor supervivencia, “representa un cambio importante en nuestro conocimiento del síndrome.”
En conclusión, los autores afirman que el principal mecanismo patogenético en el SHR tipo 1 es un deterioro potencialmente reversible de la función circulatoria sistémica, sobre todo debido a la vasodilatación esplácnica y a la vasoconstricción renal, con frecuencia desencadenadas por un factor precipitante. Además de la insuficiencia renal, el síndrome puede asociarse con otras disfunciones orgánicas, como el descenso del gasto cardíaco, la insuficiencia renal y la encefalopatía.
Mecanismos patogenéticos del síndrome hepatorrenal
SRAA: sistema renina-angiontensina-aldosterona; PBE: peritonitis bacteria espontánea
Tratamiento del síndrome hepatorrenal
Se han desarrollado nuevos tratamiento del SHR para expandir el volumen sanguíneo cerebral aumentando al mismo tiempo el volumen plasmático y reduciendo la intensa vasodilatación periférica. Los autores sostienen que esta estrategia no es enteramente nueva, ya que en 1967, Tristani y Cohn demostraron que la infusión de dextrano mejoraba el gasto cardíaco y la perfusión renal en los pacientes cirróticos oligúricos. Dieciocho años después, Shapiro y col. demostraron que, en los pacientes cirróticos con ascitis, la excreción de agua y sodio por orina mejoraba con la administración de noradrenalina y las maniobras destinadas a expandir el volumen sanguíneo central (inmersión en agua). Sin embargo, los resultados de importancia clínica solo se han obtenido recientemente con el uso de albúmina y vasoconstrictores. El mecanismo por el cual los vasoconstrictores y la albúmina mejoran el índice de filtración glomerular (IFG) en pacientes con SHR no se conoce bien. Sin embargo, la administración de terlipresina a pacientes con SHR aumenta la presión sanguínea y provoca un descenso importante de la actividad de la renina plasmática, y un aumento del IFG, lo que en forma indirecta indica que se produce una corrección de la disfunción circulatoria.
Es posible que los análogos de la vasopresina provoquen vasoconstricción del lecho esplácnico, permitiendo así la redistribución del volumen sanguíneo a ciertos órganos extraesplácnicos, incluyendo el compartimiento central y los riñones. El relleno del compartimiento central provoca la inhibición de los sistemas nervioso simpático y renina angiotensina, inclinando la curva autorreguladora hacia la izquierda y haciendo que el flujo sanguíneo renal y el IFG respondan más a las modificaciones de la presión arterial. Tradicionalmente, la albúmina siempre ha sido considerada un recurso para mejorar la función circulatoria en la cirrosis, a través de la expansión del volumen sanguíneo central y el aumento del gasto cardíaco. En general, los últimos estudios han demostrado que la administración de albúmina a pacientes cirróticos con PBE causa vasoconstricción arterial e hipertensión arterial, probablemente por la capacidad de la albúmina de unirse a los vasodilatadores. Por lo tanto, expresan los autores, es posible que una mejoría de la función renal en los pacientes con SHR tratados con vasoconstrictores y albúmina se deba a los efectos sumados que tienen los dos compuestos sobre la circulación arterial periférica.
Profilaxis del síndrome hepatorrenal
Basados en los resultados de algunos estudios, los autores sostienen que la profilaxis con albúmina debería quedar restringida a los pacientes con SHR tipo 1 y PBE, pero se requieren estudios para definir mejor la dosis óptima.
Vasoconstrictores y albúmina
Hace ya 35 años se propuso el uso de un análogo de la vasopresina para mejorar el flujo sanguíneo renal en los pacientes cirróticos. Se ha comprobado que la infusión de ornipresina mejora moderadamente el IFG, pero el fármaco fue infundido solo 4 horas, lo que no permitió la evaluación de los efectos a largo plazo. Otros dos estudios demostraron que la administración prolongada (1 a 2 semanas) de ornipresina combinada con albúmina o dopamina, normalizó la creatininemia en muchos pacientes con SHR de tipo 1. Es de destacar que la recurrencia de la insuficiencia renal solo ocurrió después de la suspensión del tratamiento, y en los pocos casos en los que se reinstaló un segundo curso terapéutico, el resultado fue exitoso. Sin embargo, dicen, el efecto adverso más frecuente de la ornipresina fue la complicación isquémica.
Por lo tanto, la difusión del uso clínico de los vasoconstrictores en pacientes con SHR solo tuvo lugar con el advenimiento de compuestos más seguros como la terlipresina, un análogo de la vasopresina con actividad más prolongada, y el agonista α2 midodrina combinado con octreotida. Los estudios sobre el uso de terlipresina muestran que:
a) aunque el IFG raramente alcanza niveles normales, un período corto de tratamiento con terlipresina mejora la función renal hasta en el 65% de los pacientes con SHR tipo 1
b) es probable que la efectividad de la terlipresina aumente con la albúmina
c) en casi el 20% de los pacientes, el SHR ocurre luego de la suspensión del tratamiento, pero su reinstauración suele ser efectiva
d) en la mayoría de los casos, la hiponatremia por dilución asociada con el SHR mejora con el tratamiento con terlipresina
e) los efectos colaterales graves del tratamiento no son comunes (5-10%).
Con respecto a la supervivencia, los pacientes que se recuperaron por completo de su SHR tipo 1 por efecto de la terlipresina tienen una mejoría de la supervivencia en el corto plazo, aunque otros estudios comprobaron que las supervivencias a los 60 días del seguimiento de pacientes tratados con terlipresina más albúmina y los tratados solo con albúmina eran iguales. Por lo tanto, faltan estudios sobre la supervivencia a largo plazo. Sin embargo, el uso de terlipresina para mejorar la función renal es un recurso de apoyo importante para los pacientes con SHR tipo 1 incluidos en listas de espera para trasplante hepático. En muchos trabajos, la dosis de terlipresina oscila entre 0,5 y 1 mg/4-6 horas. Este régimen se mantuvo hasta la reversión del SHR, la cual ocurrió hacia la segunda semana de tratamiento. En otros estudios, la dosis inicial para pacientes sin una respuesta rápida fue 2 mg/4-6 horas. La dosis diaria de albúmina fue de 20 a 40 g, precedida en algunos estudios por una carga de 1g/kg de peso corporal. Algunos consideran la presión venosa central para establecer y titular las dosis de albúmina y prevenir la sobrecarga líquida.
La experiencia con midodrina es más limitada. Hasta el momento, solo hubo dos estudios piloto en los que se uso la midodrina combinada con octreotida para mejorar el efecto de la vasoconstricción esplácnica, pero las dosis y las vías de administración fueron bastante diferentes. Dado que la octreotida sola no influye sobre el IFG en los pacientes con SHR, se deduce que la acción más importante sobre el IFG proviene de la
midodrina.
Un estudio piloto estudió la acción de una infusión de noradrenalina combinada con albúmina y furosemida con buenos resultados. La noradrenalina es más barata y disponible que la terlipresina, pero se cree que tiene mayor tendencia a inducir arritmias cardíacas. Por lo tanto, el papel de la noradrenalina en pacientes con SHR tipo 1 requiere más estudios, sobre todo comparativos con la terlipresina o la combinación de midrodrina y octreotida.
El efecto del SPIT ha sido poco estudiado en el SHR. De los trabajos consultados, surge que:
a) en la mayoría de los pacientes con SHR tipo 1, después del SPIT se nota una supresión pronunciada de los sistemas vasoactivos endógenos, en particular del sistema renina angiotensina, y un descenso de los niveles de creatinina. El descenso de la creatinina fue más lento que cuando se utiliza terlipresina más albúmina.
b) la recurrencia del SHR fue rara, siempre que el shunt funcionara bien.
c) la encefalopatía hepática fue una complicación frecuente del SPIT pero fue manejada adecuadamente con tratamiento médico.
d) el SPIT casi siempre indujo una reducción del volumen de la ascitis.
e) la resolución del SHR tipo 1 por el SPIT puede mejorar la supervivencia.
f) el tratamiento secuencial con vasoconstrictores y albúmina seguido de SPIT podría utilizarse como un tratamiento alternativo para aumentar la probabilidad de beneficios a largo plazo.
g) aunque el SPIT puede mejorar la función renal y la ascitis refractaria en pacientes con SHR tipo 2, su efecto sobre la supervivencia todavía no ha quedado establecido.
Sin embargo, dado que casi todos los estudios excluyeron a los pacientes con antecedentes de encefalopatía grave, bilirrubinemia > 5 mg/dL, o un puntaje de Chile-Pugh >12, la aplicabilidad del SPIT puede ser más que limitada en los pacientes con SHR, quienes frecuentemente presentan ictericia, encefalopatía y puntaje elevado de Chile-Pugh. Existe poca investigación sobre el mecanismo por el cual el SPIT ejerce efectos beneficiosos en pacientes con SHR. Sin embargo, como el SPIT funciona como un shunt portocava látero-lateral, se espera que alivie la hipertensión portal, la cual representa un papel importante en la patogénesis de la vasodilatación arterial esplácnica. En general, el SPIT se asocia con mayor gasto cardíaco y la expansión del volumen sanguíneo central.
Diálisis de albúmina extracorpórea
Este procedimiento utiliza un líquido de diálisis con albúmina, libre de células, que es recirculado y prefundido a través de carbón y columnas de intercambios aniónico. El sistema también está conectado a un aparato de hemodiálisis o de hemoperfusión. De este modo se pueden eliminar sustancias unidas a la albúmina, como la bilirrubina, los ácidos biliares, los aminoácidos aromáticos, los ácidos grasos de cadena mediana y las citocinas. Hay pocos datos sobre la aplicación de este método en pacientes con SHR, y los mismos son controvertidos. Es un método muy costoso y todavía debe ser considerado experimental.
Trasplante de hígado en pacientes con síndrome hepatorrenal
El trasplante hepático fue el único tratamiento efectivo para los pacientes con SHR antes de la introducción de los vasoconstrictores y el SPIT, siendo todavía el tratamiento de elección para esos pacientes. Inmediatamente después del trasplante puede haber un empeoramiento del IFG y muchos pacientes requieren diálisis por muchos tiempo (35% de los pacientes trasplantados con SHR vs 5% de los pacientes trasplantados sin SHR). Los inhibidores de la calcineurina (ciclosporina y tacrolimus) pueden contribuir al empeoramiento del IFG. Luego, el IFG comienza a mejorar hasta alcanzar valores de 30 a 40 mL/min, 1 a 2 meses después de la operación. Esta insuficiencia renal moderada persiste durante el seguimiento y probablemente se deba a un mayor efecto nefrotóxico de los inhibidores de la calcineurina en pacientes con deterioro renal pretrasplante. En efecto, expresan los autores, las anormalidades hemodinámicas y neurohormonales asociadas con el SHR desaparecen en los primeros meses postrasplante y los pacientes recuperan su capacidad para excretar sodio y agua libre. Los pacientes con SHR que han recibido un trasplante hepático tienden a tener más complicaciones, estar más tiempo internados en Terapia Intensiva y mayores tasas de mortalidad intrahospitalaria que los pacientes con trasplante hepático sin SHR. No obstante, su supervivencia a los 3 años es aceptable (60% vs 70-80 en pacientes trasplantados hepáticos sin SHR).
La principal limitación del trasplante hepático es que debido a la escasez de donantes de órganos, y su extremadamente corta supervivencia, la mayoría de los pacientes con SHR tipo 1 muere antes del trasplante. La introducción del modelo de enfermedad hepática terminal para priorizar el órgano a ser trasplantado ha solucionado en parte este problema, ya que los pacientes con SHR tienen una alta prioridad en las listas de espera. Por otra parte, el tratamiento con vasoconstrictores y albúmina del SHR tipo 1 puede mejorar la supervivencia del paciente y, por lo tanto, mejorar su probabilidad de ser trasplantado.
1314
El mayor conocimiento de los mecanismos que subyacen el SHR y el desarrollo de estrategias terapéuticas nuevas son las razones para el nuevo consenso sobre la definición, criterios diagnósticos y tratamiento del SHR organizado por el International Ascites Club.
Nuevas definiciones del síndrome hepatorrenal
El SHR es un síndrome potencialmente reversible que ocurre en pacientes con cirrosis, ascitis e insuficiencia hepática, como así en pacientes con insuficiencia hepática aguda o hepatitis alcohólica. Se caracteriza por deterioro de la función renal, alteraciones marcadas de la función cardiovascular e hiperactividad de los sistemas nervioso simpático y renina angiotensina. La vasoconstricción renal intensa provoca un descenso del IFG. Existen dos tipos de SHR. El SHR de tipo 2 se caracteriza por una insuficiencia renal moderada (creatininemia 1,5 a 2,5 mg/dL), con un curso estable o lentamente progresivo. Aparece en forma espontánea pero también por un evento precipitante. El tipo 2 se asocia generalmente con ascitis refractaria. La supervivencia de los pacientes de este grupo es más corta que la de los cirróticos no urémicos con ascitis, pero mejor que la de los pacientes con SHR tipo 1.
El SHR de tipo 1 se caracteriza por insuficiencia renal rápidamente progresiva definida por la duplicación de las concentraciones de creatinina sérica hasta un nivel mayor a 2,5 mg/dL, en menos de 2 semanas. Aparece en forma espontánea, pero suele desarrollarse luego de un evento precipitante, en particular la PBE. Suele ocurrir en el contexto de un deterioro agudo de la función circulatoria, caracterizado por hipotensión arterial y activación de los sistemas vasoconstrictores endógenos. Puede asociarse con insuficiencia cardíaca y hepática como así con encefalopatía. El pronóstico del tipo 1 es muy malo. Las diferencias principales con la definición de 1996 son:
a) la potencial reversibilidad del SHR sin trasplante hepático;
b) el papel dominante del lecho esplácnico en la vasodilatación arterial;
c) la participación frecuente de la PBE como un evento precipitante en el SHR tipo 1;
d) el concepto de que, además de la insuficiencia renal, es frecuente la insuficiencia concomitante de otros órganos, en particular el corazón;
Criterios diagnósticos revisados del síndrome hepatorrenal
Debido a que no existen características especificas del SHR, el diagnóstico se basa en la exclusión de otros tipos de insuficiencia renal. Los criterios necesarios para diagnosticar el SHR son los siguientes:
Nuevos criterios diagnósticos para el síndrome hepatorrenal en la cirrosis
|
⇒ Cirrosis con ascitis ⇒ Creatininemia 1,5 mg/dL ⇒ El nivel de creatinina sérica no disminuye después de 2 días de haber suspendido el diurético y la expansión de volumen con albúmina. La dosis de albúmina recomendada es 1 g/kg de peso corporal hasta un máximo de 100 g/día. ⇒ Ausencia de shock ⇒ Sin tratamiento actual o reciente con fármacos nefrotóxicos |
⇒ Ausencia de neuropatía parenquimatosa, indicada por la proteinuria >500 mg/día, microhematuria (> 50 eritrocitos por campo de alto aumento) y/o ecografía renal anormal |
Las principales diferencias entre esos criterios y los establecidos con anterioridad son:
a) el clearance de creatinina ha sido excluido por que es más complicado en la práctica que el uso de la creatininemia simple y no aumenta la precisión del cálculo de la función renal en los pacientes cirróticos.
b) en la actualidad, se considera SHR a la insuficiencia renal en presencia de infección bacteriana pero en ausencia de shock séptico. Esto significa que el tratamiento del SHR debe iniciarse sin esperar a la recuperación completa de la infección.
c) la expansión del volumen plasmático debe realizarse con albúmina más que con solución salina.
d) se han eliminado los criterios diagnósticos menores por no ser esenciales.
Tratamiento del síndrome hepatorrenal
La mayoría de los datos disponibles hasta el momento sobre el tratamiento del SHR provienen de análisis retrospectivos, estudios piloto, estudios comparativos no aleatorizados y solo uno pocos trabajos controlados y aleatorizados. Por otra parte, la mayoría de los estudios han incluido demasiado pocos pacientes. Por lo tanto, aclaran los autores, los conceptos y las recomendaciones prácticas que aparecen en esta parte del artículo están basados en datos publicados y en la experiencia personal de los panelistas, y puede ser mejorada a medida que se acumule más experiencia.
Prevención del síndrome hepatorrenal
La incidencia del SHR en pacientes con PBE puede reducirse con la administración de albúmina, prevención ésta que se asocia con un alargamiento de la supervivencia. La dosis de albúmina sugerida es de 1,5 g/kg de peso corporal, el primer día, seguido en el tercer día por 1 g/kg de peso corporal, hasta un máximo de 150 a 100 g, respectivamente. La administración de albúmina está indicada en los pacientes con PBE y bilirrubinemia (4 mg/día) o creatinina sérica (> 1 mg/dL). Se requieren más estudios para determinar la dosis óptima de albúmina y al subgrupo de pacientes en quienes el tratamiento está muy indicado.
Tratamientos efectivos del síndrome hepatorrenal
Trasplante de hígado
Éste es el tratamiento de elección para ambos tipos de SHR. La morbilidad luego del trasplante hepático es superior en los pacientes con SHR que en los pacientes sin SHR, aunque la probabilidad a largo plazo de supervivencia es solo algo menor. La inversión del SHR tipo 1 mediante el tratamiento farmacológico antes del trasplante hepático puede mejorar la supervivencia después del trasplante. La reducción de la creatinina sérica luego del tratamiento y la disminución relacionada del puntaje de la hepatopatía no cambia la decisión de realizar el trasplante hepático, ya que el pronóstico luego de la recuperación del SHR tipo sigue siendo muy malo.
Tratamiento farmacológico con vasoconstrictores
Los estudios sobre el tratamiento farmacológico del SHR se han realizado principalmente en pacientes con SHR tipo 1, siendo la terlipresina es el compuesto más estudiado. Su dosis inicial es de 1 mg/4-6 horas, y si no hay respuesta (>25% de disminución de la creatininemia luego de 2 días), se puede duplicar la dosis cada 2 días, hasta un máximo de 12 mg/día. El tratamiento puede detenerse cuando la creatinina sérica no disminuye al menos 50% luego de 7 días de la dosis máxima o, si no se produce el descenso luego de los primeros 3 días. En los pacientes con respuesta inmediata, el tratamiento debe continuarse hasta la reversión del SHR o hasta un efecto máximo de 14 días. La terlipresina puede inducir isquemia y arritmias lo que obliga a suspender su aplicación. Otros vasoconstrictores son la midodrina o la noradrenalina.
Para adaptar las dosis de vasoconstrictores, además de la creatininemia se pueden utilizar la presión arterial, la excreción renal de agua y sodio y la natremia. La administración de albúmina puede mejorar el efecto de los vasoconstrictores. La albúmina se debe suspender cuando su concentración sérica supera los 45 g/L o en presencia de edema pulmonar.
En respuesta al tratamiento con vasoconstrictores y albúmina se pueden esperar tres tipos de respuesta: la respuesta completa ocurra en el 60% de los pacientes tratados con terlipresina, pudiendo mejorar la supervivencia. Puede haber una recaída de la insuficiencia renal puede luego de la suspensión del tratamiento pero un nuevo tratamiento suele ser efectivo. Por el contrario, la respuesta parcial a menudo es seguida por una recaída grave e irreversible de la insuficiencia renal.
Stent-shunt portosistémicos intrahepáticoa transyugular
Los pocos datos existentes sobre los resultados del SPIT en el SHR muestran que mejora la función renal y elimina la ascitis. En los pacientes con SHR tipo 1, el SPIT puede mejorar la supervivencia pero es su resultado es dudoso en el SHR tipo 2. La mayor desventaja del SPIT es su baja aplicabilidad ya que puede usarse en pacientes con bilirrubinemias mayores de 5 mg/dL, encefalopatía grave o el antecedente de encefalopatía recurrente, infección bacteriana grave, disfunción cardíaca o pulmonar grave o puntaje de Chile-Pugh >11.
Recomendaciones finales para el tratamiento de los pacientes con síndrome hepatorrenal
SHR tipo 1
El tratamiento de primera línea es el uso de vasoconstrictores combinados con albúmina. Los pacientes que no responden a los vasoconstrictores o lo hacen parcialmente pueden ser tratados con SPIT. Si hay contraindicaciones para el SPIT, se puede recurrir a la diálisis de albúmina extracorpórea, en el contexto de estudios prospectivos.
El uso secuencial de vasoconstrictores más albúmina y SPIT en pacientes elegibles es una idea interesante para proseguir las investigaciones.
SHR tipo 2
No hay datos definitivos que avalen el uso de vasoconstrictores en estos pacientes., El SPIT puede usarse para mejorar la ascitis refractaria, la cual es frecuente en el SHR tipo 2. Poco se sabe sobre el efecto del SPIT sobre la supervivencia a largo plazo.
Conclusiones de la reunión de consenso
|
⇒ La infusion de albúmina evita el SHr en pacientes con PBE ⇒ Los vasoconstrictores y la albúmina se recomiendan como tratamiento de primera línea para el SHR tipo 1. La terlipresina es el vasoconstrictor más usado. La midodrina + octreotida y noradrenalina son dos alternativas posibles que requieren más evaluación clínica. ⇒ Con el uso de la terlipresina (2-12 mg/día) y albúmina (20-40 mg/día después de 1 g/Kg el primer días) cerca del 60% de los casos de insuficiencia renal se recuperan. La mejoría de la supervivencia usando solo vasoconstrictores y albúimina es más que limitada. ⇒ El SPIT es un tratamiento alternativo en pacientes adecuados, en especial en aquellos que responden parcialmente a los vasoconstrictores, pero también puede usarse en pacientes con una respuesta completa de los niveles de creatinina a la eliminación de la ascitis y para mantener la función renal normal. ⇒ El trasplante de hígado es el único tratamiento que asegura una supervivencia prolongada. |
⇒ El tratamiento farmacológico y el SPIT pueden servir durante el tiempo de espera para el trasplante hepático y para mejorar la supervivencia postrasplante. |